In den letzten Jahren wurden einige therapeutische Ansätze für chronische Wunden neu oder weiterentwickelt. Lösungen zum enzymatischen Debridement auf Bromelaïn-Basis bei Ulcus cruris stehen kurz vor der Zulassung, rekombinant erzeugte Maden-Enzyme zum Debridement werden untersucht, genauso wie Phagen als Waffe gegen bakterielle Infektion und Betablocker für die Wundheilung.
Debridement mit Enzymen
Gerade die Techniken des Debridements haben sich in den letzten Jahren deutlich entwickelt. Statt des schmerzhaften mechanischen Debridement kann heute totes Gewebe enzymatisch entfernt werden.
Bromelain
Eines dieser Enzyme ist Bromelaïn, das aus dem Stamm der Ananas-Pflanze gewonnen wird. Für das enzymatische Debridement bei Brandverletzten ist ein Präparat (NexoBrid®, PolyMedics Innovations) bereits in der EU zugelassen. Das Gel wird auf die Wunden aufgetragen und innerhalb eines Tages löst sich der Verbrennungsschorf auf, deutlich schneller als bei der Standardbehandlung. In einer kleinen Pilotstudie an Patienten mit offenen Beinen ließ sich das nekrotische Gewebe mit dem Gel innerhalb von 24 Stunden vollständig entfernen. Für eine Zulassungserweiterung sind Studien mit größerer Teilnehmerzahl erforderlich.
Für die Behandlung von Ulcus cruris ist ein zweites Bromelaïn-Präparat in der Pipeline (Eschar-Ex®, MediWound). In einer aktuellen Studie wurden 119 Ulcus cruris-Patienten mit dem Bromelaïn-Gel, Placebo oder einer nicht-chirurgischen Standardtherapie behandelt. In der Verumgruppe erreichten zwei Drittel innerhalb von acht Tagen ein vollständiges Debridement, in der Placebo-Gruppe waren es 30 Prozent, in der Standard-Care-Gruppe 14 Prozent. In einer weiteren kleinen Studie löste das Präparat nicht nur Nekrosen auf, sondern reduzierte den Biofilm und die Bakterienlast der Wunden. Am Ende der Beobachtungszeit war nach zwei Wochen die Wundfläche um 35 Prozent verkleinert.
Maden-Enzyme
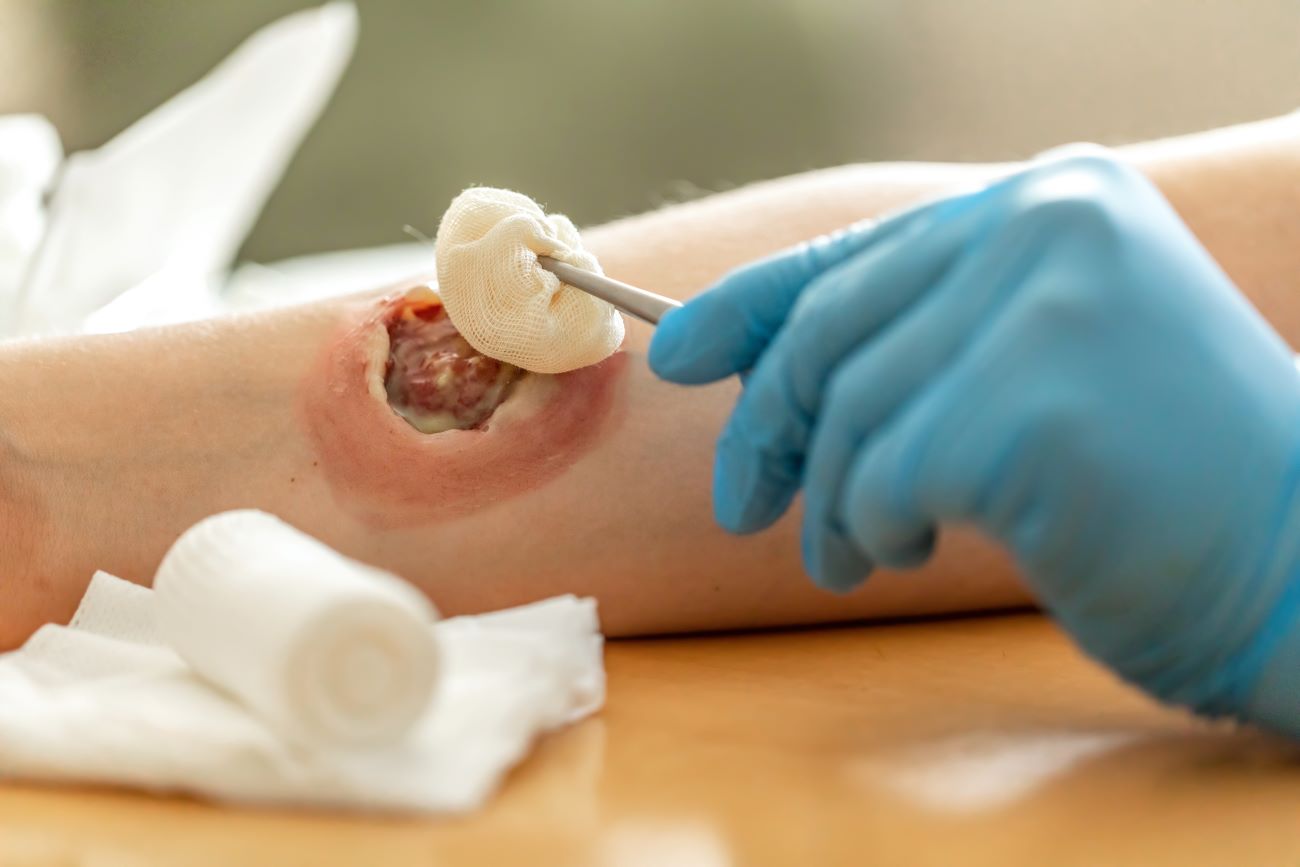
Eine kleine Renaissance scheint das Debridement mittels Enzymen tierischen Ursprungs zu erfahren – jedoch in veränderter Form. In den 1990er Jahren war die Auflösung des Wundbelags durch Maden en vogue. Die Fliegenmaden wurden in kleinen Gaze-Säckchen auf die Wunden gelegt, lösten das nekrotische Gewebe enzymatisch auf und hinterließen einen sauberen Wundgrund. Verständlicherweise war die Akzeptanz dieser Therapie nicht groß. Heute wird die Trypsin-Serin-Protease der Maden (Tarumase) mit selektiver Aktivität gegen Fibrin, Kollagen und Elastin aus medizinischen Maden gewonnen. Nicht-klinische Studien haben ergeben, dass es selektiv Fibrin auflöst und die bakterielle Belastung des Wundbetts verringert. Erste klinische Studien brachten keine Hinweise auf systemische Resorption, Bildung von Antikörpern oder systemische Auswirkungen auf die Gerinnungswege. Lokale Schmerzen oder Juckreiz traten nicht auf, Erytheme, Ödeme, Exsudat oder Blutungen nahmen nicht zu. Stattdessen wurden die Wunden schneller debridiert und nach vier Wochen konnten auch Trends zur Abheilung beobachtet werden: Es bildete sich mehr Granulationsgewebe und die Wundfläche verringerte sich.
Phagen gegen Bakterien
Bei der Phagen-Therapie werden gegen die pathogenen Bakterien gerichtete Phagen in einer Lösung auf die Wunde aufgebracht, die die Pathogene zerstören. Auch wenn fast 80 Prozent der Erreger in chronischen Wunden auf Staphylococcus aureus und Pseudomonas aeruginosa entfallen, sollten vor der Therapie die betreffenden Keime identifiziert werden, um die wirksamen Bakteriophagen zu ermitteln und ein Phagogramm erstellen zu können. Mit dessen Hilfe kann ein maßgeschneiderter Phagen-Cocktail zusammengestellt werden. Die Phagen-Therapie hat sich in mehreren Studien als erfolgreich erwiesen: In einer indischen Studie wurden die chronischen Wunden von Patienten mehrmals mit der Phagen-Lösung gespült, bis die Wunde frei von infizierenden Bakterien war. Nach drei Monaten waren die Wunden bei 81 Prozent der Patienten frei von pathogenen Keimen, bei den Diabetikern waren es 74,1 Prozent.
Topische Betablocker für die Wundheilung
Scheinbar können auch Betablocker die Wundheilung fördern: Erste Versuche mit Timolol-enthaltenden Augentropfen waren vielversprechend. Inzwischen sind auch die pathophysiologischen Mechanismen entschlüsselt: Weichteilschäden lassen sympathische Nerven große Mengen an Katecholaminhormonen freisetzen, über ß-adrenerge Rezeptoren die Wundheilung beeinträchtigen. Betablocker hemmen spezifisch die Aktivierung von ß-adrenergen Rezeptoren und beschleunigen darüber hinaus die Wundheilung des Weichgewebes.
In einer Placebo-kontrollierten Untersuchung wurden Ulcus cruris-Patienten 12 Wochen mit einem Timolol-Gel oder Standardtherapie behandelt. In Woche 12 war bei 67 Prozent der Timolol-behandelten Patienten die Ulkusfläche um ≥40 Prozent reduziert, unter Standardtherapie waren es 32 Prozent.
Eine Metaanalyse zu topischem Timolol bei chronischen Wunden kommt zu dem Schluss, dass der Wirkstoff als wirksame und sichere Zusatzbehandlung für refraktäre Wunden, vor allem venöse Beingeschwüre und diabetische Fußgeschwüre, gewertet werden kann. Die Anwendung ist einfach und kostengünstig, aber noch Off-Label, Zulassungsstudien sind bereits in Arbeit.
Bericht: Angelika Ramm-Fischer
Bildquelle:© Annabell-Gsoedl – stock.adobe.com