Genetik in der Präzisionsmedizin verändert die moderne Kardiologie grundlegend. Genetische Erkenntnisse ermöglichen heute nicht nur präzisere Diagnosen, sondern eröffnen völlig neue Therapieansätze bei Herzerkrankungen. Auf der MEDICA 2025 in Düsseldorf zeigten führende Experten, wie genetische Informationen zunehmend für die breite Bevölkerung nutzbar werden – von seltenen Erbkrankheiten bis zu häufigen Volksleiden.
MEDICA-Session: Genetik als Motor der Präzisionsmedizin
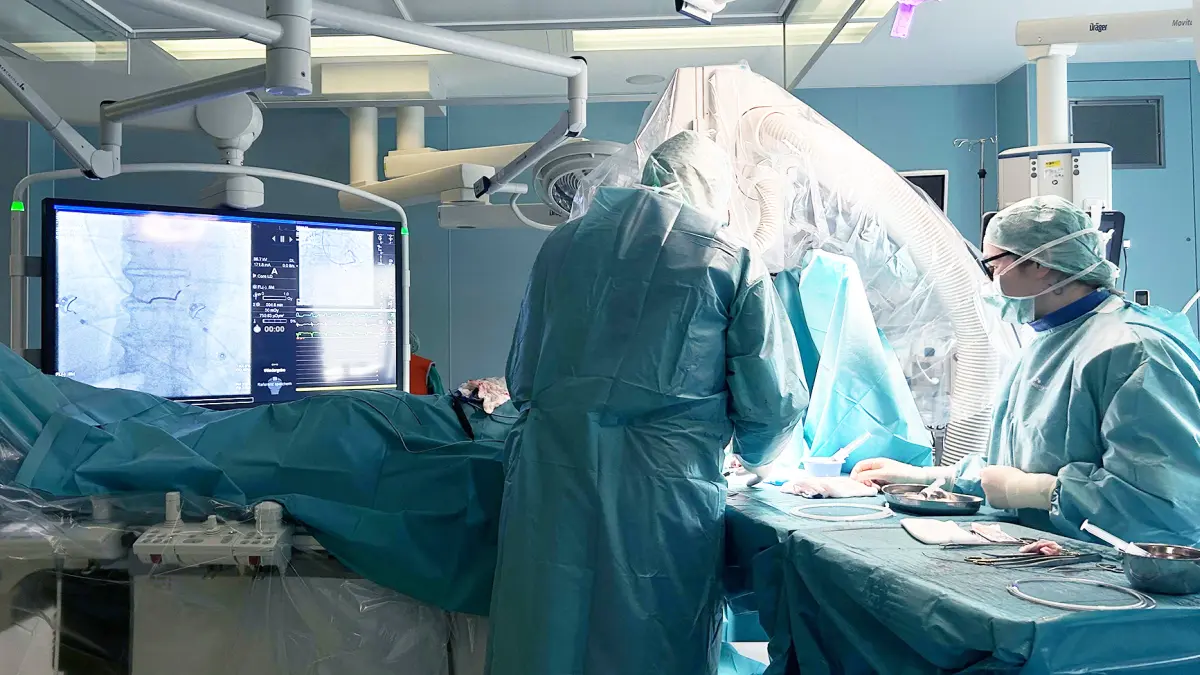
Die moderne Kardiologie profitiert immer mehr von genetischen Erkenntnissen sowohl in der Diagnostik als auch in der Prävention und Therapie. Auf der MEDICA in Düsseldorf, einer Fachmesse für Medizintechnik, Medizinprodukte, Elektromedizin, Labortechnik und Diagnostika, berichteten im November 2025 mehrere Experten im Labmed-Forum, wie genetische Informationen für die breite Bevölkerung genutzt werden können.
Genetische Mechanismen bei Herzmuskelerkrankungen
Prof. Dr. med. Cordula Wolf, Leiterin des Zentrums für seltene angeborene Herzerkrankungen und Kardiogenetik am Deutschen Herzzentrum München, gab zunächst einen komprimierten Überblick über die genetischen Mechanismen hereditärer Herzmuskelerkrankungen. Anhand ausgewählter Fälle zeigte sie, wie genetische Diagnosen zunehmend therapeutische Konsequenzen haben.
Beispiel: Hypertrophe Kardiomyopathie
Sie skizzierte die Fortschritte bei der hypertrophen Kardiomyopathie, die oft durch Mutationen in sarcomeren Proteinen wie z. B. MYBPC3 verursacht wird. Auch wenn klassische Behandlungsansätze wie ICD-Implantation oder die Beseitigung hämodynamischer Obstruktionen weiterhin zentral bleiben, eröffnet die therapeutische Hemmung der Myosin-Aktin-Interaktion inzwischen eine erstmals kausale pharmakologische Option.
Wichtige Entwicklungen:
- Myosin-Inhibitoren verändern direkt den zellbiologischen Mechanismus
- Sie wirken der Myokardhypertrophie entgegen
- Markieren einen wichtigen Paradigmenwechsel in der Behandlung
Genetische Diagnostik bei pädiatrischen Erkrankungen
Wolf stellte zudem kompakt dar, wie bei seltenen syndromalen Formen wie dem Noonan-Syndrom, ausgelöst durch Störungen im RAS-MAPK-Signalweg, der Einsatz von MEK-Inhibitoren, ursprünglich aus der Onkologie, schwere kardiale Verläufe beeinflussen kann.
Therapeutische Durchbrüche:
- MEK-Inhibitoren bei Noonan-Syndrom
- Erste gentherapeutische Ansätze bei Danon-Erkrankung
- Genetik in der Präzisionsmedizin eröffnet direkte therapeutische Optionen bei pädiatrischen Erkrankungen
„Genetische Diagnosen klären heute nicht mehr nur die Krankheitsursache, sondern sind häufig der Schlüssel zu zuvor unvorstellbaren Therapieoptionen”, so Wolf.
Polygenic Risk Scores (PRS) – Genetik für die Allgemeinbevölkerung
PD Dr. med. Teresa Trenkwalder vom Deutschen Herzzentrum München widmete sich der Frage, wie genetische Erkenntnisse jenseits seltener monogener Erkrankungen für die Allgemeinbevölkerung nutzbar werden können.
Wie entstehen kardiovaskuläre Volkskrankheiten?
Sie stellte heraus, dass der überwiegende Teil der kardiovaskulären Volkskrankheiten nicht von einzelnen Mutationen ausgelöst wird:
Unterschied monogene vs. polygene Erkrankungen:
- Monogene Erkrankungen: Einzelne Mutationen mit starken, klar erkennbaren Effekten (z. B. hypertrophe Kardiomyopathie, Marfan-Syndrom)
- Polygene Erkrankungen: Resultat zahlreicher genetischer Varianten mit kleinen individuellen Effekten (z. B. koronare Herzkrankheit, Vorhofflimmern)
- Risikoverteilung: Bei häufigen Erkrankungen verteilt sich das Risiko auf viele 100 bis 1.000 genetische Positionen
Was sind Polygenic Risk Scores?
Polygenic Risk Scores (PRS) erfassen das genetische „Gesamtgewicht” eines Individuums für eine bestimmte Erkrankung. Trenkwalder erläuterte Schritt für Schritt, wie PRS berechnet werden:
Berechnungsschritte:
- Chip-basierte Genotypisierung
- Statistische Imputation fehlender SNPs
- Identifikation signifikanter Risikoloci mittels Manhattan-Plots
- Zusammenführung zu einem individuellen Score
Anhand bestehender genomweiter Assoziationsstudien (GWAS) zeigte sie, wie über 300 Risikovarianten für die koronare Herzkrankheit identifiziert wurden.
Wie funktionieren GWAS-Studien?
Grundlage sind groß angelegte GWAS mit Hunderttausenden Probanden, in denen die Häufigkeit bestimmter genetischer Varianten bei Erkrankten und Gesunden verglichen wird.
„Varianten, die in einer Gruppe deutlich häufiger auftreten, gelten als Risikoloci. Mittlerweile sind allein für die koronare Herzkrankheit über 300 solcher Risikovarianten bekannt”, berichtete Trenkwalder.
So entsteht der persönliche Risikowert:
- Für jede Variante wird die Stärke ihres Effekts („Gewicht”) berechnet
- Alle Varianten eines Individuums werden zu einem Score aufsummiert
- Es entsteht ein persönlicher genetischer Risikowert, der ein Leben lang konstant bleibt
Integration in die klinische Praxis
Besonders anschaulich zeigte die Expertin, dass der PRS nicht im luftleeren Raum existiert, sondern in ein klinisches Gesamtkonzept eingebettet sein muss. Sie betonte, dass der Score weder alleiniges Diagnoseinstrument noch alleiniger Therapieentscheider sein darf.
Wann ist ein PRS sinnvoll?
Wenig Zusatznutzen bei:
- Menschen mit erheblichen klassischen Risikofaktoren (massiv erhöhte LDL-Werte, Hypertonie, Rauchen)
- Sehr risikoarmen Personen ohne unmittelbare medizinische Konsequenz
Maximaler Nutzen bei:
- Patienten mit intermediärem Risiko
- Präzisere Einordnung möglich
- Frühzeitigere präventive Behandlung
- Intensivere Überwachung
Zielgruppe: Patienten mit intermediärem Risiko
Die entscheidende Zielgruppe seien daher Patienten mit intermediärem Risiko. Hier könne der PRS laut Trenkwalder dabei helfen, Personen präziser einzuordnen und frühzeitiger präventiv zu behandeln oder intensiver zu überwachen.
Dies könne langfristig darüber entscheiden, ob ein Mensch mit mittlerem Risiko die Entwicklung einer manifesten koronaren Herzkrankheit vermeidet oder ob er im Verlauf zu spät einer wirksamen Prävention zugeführt wird.
Wichtige Voraussetzung: Ethnische Passgenauigkeit
Ein PRS, der auf Daten europäischer Populationen beruht, könne nicht ohne Weiteres auf asiatische oder afrikanische Bevölkerungen übertragen werden.
Zukunft der Genetik in der Präzisionsmedizin
Trenkwalder gab zudem einen Ausblick in eine Zukunft, in der polygenetische Informationen stärker mit klinischen Parametern, Bildgebung und KI-gestützten Algorithmen verschmelzen werden.
Zukünftige Entwicklungen:
- Individualisierte Risikoprofile weit über klassische Risikorechner hinaus
- Polygenetische Daten für strukturelle Herzerkrankungen (z. B. kalzifizierende Aortenklappenstenose)
- Neue Möglichkeiten für die Früherkennung
- Laufende Studien mit über 80.000 Patienten zeigen: Auch valvuläre Erkrankungen werden durch zahlreiche genetische Varianten beeinflusst
Herausforderungen der genetischen Diagnostik
Die Herausforderungen der modernen genetischen Diagnostik thematisierte Prof. Dr. med. Eric Schulze-Bahr, Direktor des Instituts für Genetik von Herzerkrankungen (IfGH) am Universitätsklinikum Münster.
Risiko der Überinterpretation
Während Sequenzierverfahren immer empfindlicher werden und eine wachsende Zahl genetischer Varianten identifizieren, steigt zugleich die Gefahr der Überinterpretation.
Problematische Entwicklungen:
- Viele Gene, die früher mit bestimmten Erkrankungen in Zusammenhang gebracht wurden, besitzen bei genauerer Prüfung keine ausreichende Evidenzbasis
- Konsortien wie ClinGen oder der PanelApp des Genomics-England-Programms ermöglichen heute eine strukturierte Bewertung
- Deutlich bessere Trennschärfe zwischen gesicherten, wahrscheinlichen und widerlegten Krankheitsgenen
Bessere Trennschärfe dank strukturierter Bewertung
Dies sei essenziell, um Fehldiagnosen zu vermeiden und Patienten nicht durch unklare Befunde zu verunsichern. Ein zentrales Problem bleibe die große Zahl an Varianten unklarer Signifikanz, die zwangsläufig bei breiter Sequenzierung auftreten und im klinischen Alltag schwer zu handhaben seien.
Warnung vor vorschneller Kommunikation:
- Varianten unklarer Signifikanz nicht vorschnell als krankheitsrelevant kommunizieren
- Moderne Sequenzierverfahren machen zunehmend sekundäre Befunde sichtbar
- Kardiologisch relevante Befunde erfordern fachkundige Einordnung
- Verantwortungsvoller Umgang mit genetischer Diagnostik ist entscheidend
Sekundäre Befunde in der Praxis
Schulze-Bahr hob hervor, dass 1,2 % der Bevölkerung im Rahmen breiter Sequenzierungen zufällig genetische Befunde erhalten, die unmittelbare therapeutische Konsequenzen haben können. Kardiologinnen und Kardiologen müssten daher zunehmend auf diese unerwarteten Konstellationen vorbereitet sein.
Autorin: Sonja Buske