Aus UroForum Heft 01/2025
Marieke Vermeulen-Spohn, Yue Che
Die robotisch-assistierte, ICG-gesteuerte Sentinel-Lymphknoten-Biopsie ist eine vielversprechende Technik mit potenzieller klinischer Relevanz für das von Keimzelltumoren des Hodens. Gegenwärtige -Methoden (CT, MRT, microRNA 371a-3p) haben eine begrenzte Genauigkeit, insbesondere bei der Früherkennung von okkulten Metastasen im klinischen Stadium I von Hodentumoren. Die RAISN-Studie (Robot-assisted Indocyanine Green-guided Sentinel Lymph Node Biopsy in Clinical Stage I Germ Cell Tumor) verfolgt einen innovativen Ansatz, bei dem die laparoskopische oder roboterassistierte Lymphknotenentfernung unter Indocyaningrün-Fluoreszenz-Bildgebung untersucht wird.
Sollte sich die Methode als vorteilhaft erweisen, könnte sie dazu beitragen, die Genauigkeit des s zu verbessern somit Überbehandlungen und die damit verbundenen toxischen Nebenwirkungen zu minimieren.
Progressionsrisiko reduzieren, Übertherapie minimieren
Die meisten Patienten mit der Diagnose eines Hodentumors präsentieren sich zunächst im klinischen Stadium I [1]. Bei diesen Patienten kommt es – abhängig vom histologischen Subtyp des Tumors – in 20–50 % der Fälle während der aktiven Überwachung zu einem Rezidiv, das häufig auf eine nicht erkannte okkulte Metastasierung zurückzuführen ist [2].
Obwohl das Langzeitüberleben von Patienten mit Hodentumoren insgesamt sehr gut ist, gehen die durch Chemotherapie und Strahlentherapie induzierten Langzeittoxizitäten mit einer erhöhten Inzidenz von Nebenwirkungen wie kardiovaskulären Erkrankungen und sekundären Malignomen einher [3–5].
Risikoadaptierte Strategien, die auf dem histologischen Befund des abladierten Hodens basieren, wurden eingeführt, um die Belastung durch adjuvante Therapien zu reduzieren. Diese Strategien haben jedoch eine geringe Sensitivität und Spezifität und führen bei einem Großteil der Patienten, die eine adjuvante Chemotherapie erhalten, weiterhin zu einer Überbehandlung [2].
Beispielsweise kann Nicht-Seminom-Patienten mit Lymphgefäßinvasion im Orchiektomiepräparat eine adjuvante Chemotherapie mit einem Zyklus Cisplatin, Etoposid und Bleomycin angeboten werden. Das Rezidivrisiko in dieser Patientengruppe liegt bei 50 %.
Das bedeutet, dass 50 % dieser Patienten eine Chemotherapie empfohlen wird, ohne dass eine okkulte Metastasierung vorliegt. Daher ist es wichtig, die diagnostischen Verfahren bei der Erstdiagnose zu verbessern, um letztlich das Risiko einer Progression der okkulten Metastasen zu reduzieren und gleichzeitig eine Übertherapie zu minimieren.
Es wurden bereits einige kleinere Studien durchgeführt, in denen die Sentinel-Lymphknoten-Diagnostik bei Hodentumorpatienten mittels radioaktiver Tracer untersucht wurde [6–8]. In diesen Studien (mit insgesamt 55 Patienten) wurden die Sentinel-Lymphknoten mit einem Technetium-basierten Tracer markiert und laparoskopisch entfernt. Die Detektion des Sentinel-Lymphknotens war bei 93–100 % der Patienten erfolgreich.
Patienten, bei denen okkulte Metastasen im Sentinel-Lymphknoten nachgewiesen wurden, erhielten eine systemische Therapie. Alle anderen Patienten wurden ohne adjuvante Therapie weiter beobachtet. Während der aktiven Überwachung traten insgesamt nur bei zwei Patienten (4 %) Rezidive auf. Die Ergebnisse dieser Pilotstudien zeigen das hohe Potenzial der Sentinel-Lymphknoten-Diagnostik beim Hodentumor.
Um den Einsatz von radioaktiven Tracern zu reduzieren und eine höhere Verfügbarkeit des Verfahrens zur ermöglichen, wird in der RAISN-Studie die Färbung der Sentinel-Lymphknoten mittels Indocyaningrün (ICG) durchgeführt. ICG hat sich bereits als Standard beim lymphonodalen in einer Reihe von Tumorerkrankungen, insbesondere bei gynäkologischen Malignomen, etabliert [9–11].
Sensitivität auf dem Prüfstand
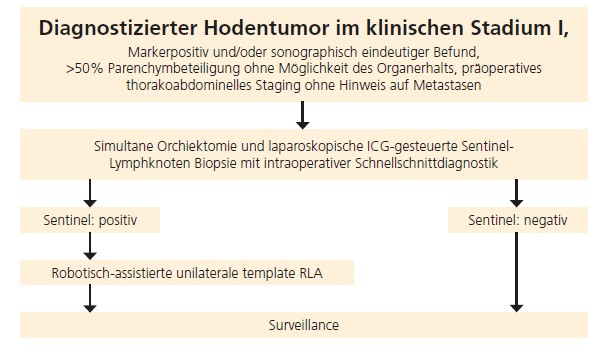
Das primäre Ziel der RAISN-Studie ist die Untersuchung der Sensitivität von der ICG-gesteuerten Sentinel-Lymphknoten-Diagnostik für das nodale im klinischen Stadium I von Hodentumorpatienten (Studiendesign ▶ Abb. 1). In dieser Phase-II-Studie ist die Rekrutierung von 27 Patienten geplant.
Volljährige Patienten, bei denen ein klinisch eindeutiger Hodentumor diagnostiziert wurde (bestätigt durch laborchemische Tumormarker, Sonographie und klinischen Tastbefund) und bei denen ein metastasiertes Krankheitsstadium durch CT-Untersuchung von Thorax und Abdomen ausgeschlossen wurde, können in die Studie eingeschlossen werden.
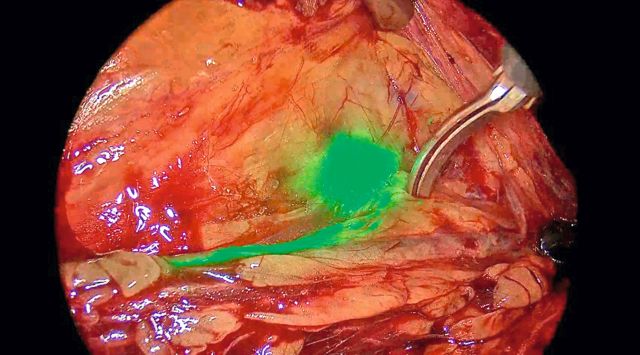
Den Patienten wird im Rahmen der inguinalen Hodenentfernung auch der Sentinel-Lymphknoten entfernt. Die Operation beginnt mit der laparoskopischen Darstellung des Retroperitoneums. Dann wird die ICG-Lösung in den betroffenen Hoden injiziert. Anschließend kann mit einer Infrarotkamera (meist nach zwei bis zehn Minuten) die Anfärbung der Lymphbahnen beobachtet werden (▶ Abb. 2). Der erste sich anfärbende Lymphknoten wird entfernt, bei simultaner Anfärbung werden auch mehrere entfernt.
Die entfernten Lymphknoten werden zur Schnellschnittdiagnostik eingesandt. Im gleichen Eingriff wird anschließend der betroffene Hoden inguinal abladiert. Nach Erhalt der Schnellschnittergebnisse wird bei negativem Befund die Operation beendet. Bei positivem Schnellschnittbefund erfolgt die robotisch-assistierte systematische retroperitoneale Lymphadenektomie (RLA) der betroffenen Seite.
Anschließend werden alle Patienten in eine strukturierte Nachsorge eingeschlossen, eine adjuvante Chemotherapie soll primär nicht erfolgen.
Das Potenzial des RAISN-Verfahrens liegt in der Möglichkeit, okkulte Metastasen mit einer hohen Sensitivität und minimalen Invasivität nachzuweisen bzw. auszuschließen. Die Notwendigkeit von Chemotherapien wird insgesamt reduziert. Erstens durch den Wegfall der adjuvanten Chemotherapien. Zweitens durch die Vermeidung von Rezidiven, indem bei positivem Sentinel eine sofortige RLA durchgeführt wird.
Für Patienten mit negativen Sentinel-Lymphknoten eröffnet sich zudem die Möglichkeit, individuellere und weniger belastende Überwachungsprotokolle zu wählen, was zu einer Verringerung der psychischen Belastung durch eine lange Nachsorge führen würde.
Ergebnisse und Ausblick
Bisher wurden 18 Patienten mit der Erstdiagnose eines Hodentumors in die RAISN-Studie eingeschlossen. Bei allen Patienten konnte laparoskopisch oder robotisch ein Sentinel-Lymphknoten nachgewiesen werden. Insgesamt traten keine Komplikationen auf. Die Patienten zeigten im Anschluss an die Operation keine höhere Krankenhausverweildauer als Patienten, bei denen eine Ablatio testis allein durchgeführt wird (ein bis zwei Tage postoperativ).
Alle Patienten werden regelmäßig in unserer Klinik nachuntersucht. Die Rekrutierung verläuft bisher sehr erfolgreich, sodass diese erweiterte Stichprobengröße realistisch in den nächsten Monaten erreicht werden kann. Die Auswertung der Ergebnisse erfolgt nach Abschluss der mindestens zweijährigen Nachbeobachtungszeit. Mit der Veröffentlichung der Ergebnisse ist daher 2027 zu rechnen.
Insgesamt hoffen wir, mit dieser Studie ein neues diagnostisches Instrument bei der Erstdiagnose eines Hodentumors zu etablieren, mit dem eine okkulte Metastasierung zuverlässig nachgewiesen oder ausgeschlossen werden kann. Dadurch könnten Hodentumorpatienten im Stadium I wesentlich gezielter behandelt und nachbeobachtet werden.
Insgesamt könnte die Anzahl der notwendigen Chemotherapien und damit deren therapieassoziierte Toxizität reduziert werden. ◼
Literatur unter www.uroforum.de

Korrespondenzadresse:
Dr. med. Yue Che
Universitätsklinikum Düsseldorf
Moorenstr. 5
40225 Düsseldorf
yue.che@med.uni-duesseldorf.de


