Die Mammakarzinom Früherkennung hat die Brustkrebsmortalität in Europa um etwa 20% gesenkt. Mindestens ein Viertel dieser Erfolge ist der rechtzeitigen Erkennung zuzuschreiben. Dieser Beitrag beleuchtet aktuelle diagnostische Verfahren, vom Mammographie-Screening bis zu innovativen Methoden wie der Digitalen Brust-Tomosynthese und künstlicher Intelligenz.
Früherkennung trägt maßgeblich zu einer Reduktion der Mortalität durch Brustkrebs bei. Als Standardmethode hat sich die digitale Mammographie (DM) durchgesetzt. Moderne Verfahren wie digitale Tomosynthese, Kontrastmittel-verstärkte Mammographie und MRT machen die Früherkennung immer besser. Was diese Methoden leisten und wie Künstliche Intelligenz die Diagnostik verändern könnte, zeigt dieser Beitrag.
Bedeutung der Mammakarzinom Früherkennung
Obwohl in Europa die Brustkrebsinzidenz in den Jahren von 1995 bis 2015 um rund 20% angestiegen ist, war gleichzeitig eine Senkung der Mortalität um ebenfalls etwa 20% zu beobachten [1]. Die Verteilung der Mortalitätssenkung zeigt deutlich die Bedeutung verschiedener Therapieansätze:
- Nur ein Sechstel der Mortalitätssenkung ist den verbesserten Therapiemöglichkeiten im metastasierten Stadium zuzurechnen [2]
- Gut die Hälfte der Mortalitätssenkung ist auf die verbesserte Therapie des Mammakarzinoms in frühen Stadien (early breast cancer) zurückzuführen [3]
- Mindestens ein Viertel der Mortalitätssenkung ist der Früherkennung zuzurechnen – je kleiner der Tumor, desto besser die Prognose
Zur Reduktion des Anteils später Tumorstadien gehört die Früherkennung früher Tumorstadien mittels verschiedener diagnostischer Verfahren, aber auch die Prävention durch Ausschaltung von Risikofaktoren (z.B. Lebensstil, Hormontherapie, Familienplanung), die Erkennung und Beratung von Frauen mit besonderem Risiko – insbesondere genetische Risiken – und ggf. Einsatz medikamentöser Prävention (z.B. bei DCIS). In diesem Beitrag soll es um die Früherkennung im engeren Sinne gehen, also die Erkennung von Vorstufen und frühen Tumorstadien.
Mammographie-Screening als Goldstandard
Im Zentrum der Mammakarzinom Früherkennung steht das organisierte Mammographie-Screening für Frauen zwischen einem Alter von 50 und 75 Jahren (LoE 1aA AGO++) [4]. Hintergrund für die Einführung des Mammographie-Screening-Programms war, dass mehrere randomisierte kontrollierte Studien einen signifikanten Überlebensbenefit für Frauen mit Mammographie-Screening gegenüber Frauen ohne Screening gezeigt hatten [5].
Ablauf des Screening-Programms
Im Rahmen des Mammographie-Screening-Programms werden die Anspruchsberechtigten gemäß Bundesmantelvertrag alle zwei Jahre zur Mammographie eingeladen. Standardverfahren ist derzeit der Einsatz der digitalen Mammographie in zwei Ebenen – eine ärztliche Untersuchung findet nicht statt.
Frauen mit auffälligen Befunden werden zu weitergehender Bildgebung (Zielaufnahmen, Ultraschall, ggf. MRT) eingeladen und bei weiter bestehendem Verdacht einer Ultraschall-gestützten oder stereotaktischen Biopsie zugeführt. Der Rate falsch-positiver Befunde und überflüssiger Punktionen sind durch Vorgaben der Qualitätssicherung für das einzelne Screening-Zentrum enge Grenzen gesetzt [6].
Erfolge des Mammographie-Screenings in Deutschland
Das gesetzliche Mammographie-Screening wurde in Deutschland seit 2005 flächendeckend eingeführt (zunächst nur für 50 bis 69-jährige) und kann als voller Erfolg gewertet werden:
- In der Zielgruppe des Mammographie-Screening-Programms (50-69-jährige) wurde die Rate fortgeschrittener Karzinome signifikant gesenkt (UICC-Stadium 3 und 4 jeweils um 20%)
- Seit Einführung des Screenings wurde eine Senkung der Brustkrebs-bezogenen Mortalität um 32% beobachtet
- Die Mortalität in den anderen Altersgruppen veränderte sich nur unwesentlich [7]
- Ähnliche Beobachtungen waren in allen europäischen Ländern zu machen [1]
Altersabhängige Empfehlungen
Der Effekt des Screenings ist von der altersspezifischen Inzidenz und Lebenserwartung abhängig. Ab einer Inzidenz von etwa 150 pro 100.000 Frauen pro Jahr kann mit einer messbaren Reduktion der Brustkrebsmortalität gerechnet werden:
- 45-49-jährige: Eine Erweiterung auch auf diese Gruppe ist zu erwarten (LoE 1aA AGO+)
- Unter 45-jährige: Die Inzidenz ist zu gering; darüber hinaus ist die Aussagekraft der Mammographie häufig wegen zu dichten Brustgewebes eingeschränkt bei zusätzlich erhöhter Empfindlichkeit des Gewebes gegenüber der Strahlenexposition
- Ab 40 Jahren: Die Strahlenschutzkommission schlägt ein Lebenszeit-Erkrankungsrisiko von 15-29% als Voraussetzung vor (LoE 1bB AGO +/-) [8]
- Über 75-jährige: Die Früherkennung mittels Mammographie muss in Bezug zur individuellen Lebenserwartung gesetzt werden (LoE 4 C AGO +/-) [4]
Eine Indikation zur Früherkennungs-Mammographie kann im Übrigen im Rahmen des intensivierten Früherkennungs- und Nachsorgeprogramms (IFNP) bei Frauen mit erblicher Belastung indiziert werden (AGO ++).
Herausforderungen und Optimierungsbedarf
Eine Herausforderung stellt unverändert die Optimierung der Sensitivität, die Reduzierung der Rate an Intervallkarzinomen und der Rate unnötiger Zusatzuntersuchungen und Punktionen dar. Auch die Vorgehensweise bei Läsionen mit unsicherem biologischen Potenzial (B3) ist stetes Ziel der Forschung und der Optimierung.
Derzeit müssen unterschiedlich viele Biopsien durchgeführt werden, um einen Brustkrebs-bedingten Tod zu verhindern:
- Bei 60-69-jährigen: 8 Biopsien
- Bei 70-75-jährigen: 13 Biopsien
- Bei 50-59-jährigen: 20 Biopsien
- Bei 40-49-jährigen: 55 Biopsien 4,9
Die digitale Mammographie (DM) ist heute das Standardverfahren. An neuen Verfahren stehen die Digitale Brust-Tomosynthese (DBT), die Kontrastmittel-verstärkte Mammographie (CEM) und der Einsatz künstlicher Intelligenz (AI) zur Verfügung.
Digitale Brust-Tomosynthese (DBT)
Bei der DBT werden durch Belichtungen aus verschiedenen Winkeln digitale Bilder aufgenommen, aus denen dann meist 1mm dicke Schichten berechnet werden. Auf diese Weise werden Überlagerungen von Läsionen durch Brustgewebe reduziert und die Erkennbarkeit deutlich verbessert. Außerdem können aus den Einzelschichten Bilder synthetisiert werden, die der klassischen Mammographie sehr nahe kommt (sog. synthetische 2D-Mammographie, S2D, SM). Diese synthetischen Mammographien erleichtern die Vergleichbarkeit mit Voruntersuchungen und durch Verzicht auf eine zusätzliche 2D-Mammographie wird Röntgendosis eingespart.
Studienergebnisse zur DBT
In drei von vier klinischen Studien war die DBT/SM der DM gegenüber überlegen:
- In einer gepoolten Analyse war die Krebserkennungsrate (CDR) in der ersten Screening-Runde signifikant besser mit der DBT (RR 1,41; 95% CI 1,20–1,64) [10]
- Nach einer weiteren Metaanalyse erscheinen die Vorteile der DBT in europäischen Studien stärker als in US-amerikanischen, möglicherweise durch die unterschiedlichen Screening-Intervalle (2 J. vs 1 J.) bedingt [5, 10]
- Die Rate an Intervallkarzinomen ließ sich dagegen kaum beeinflussen
Die deutsche TOSYMA-Studie fand durch die DBT/SM einen absoluten Anstieg früher Karzinome im Vergleich zur DM (Odds ratio 1,7; 95% C.I. 1,2–2,6) 11,12, dies betont in der Gruppe der 60-70-jährigen mit dichten Brüsten (OR 26; 95% C.I. 1,0 – 7,0).
Eine andere Studie (die piemontesische Proteus-Donna-Studie) zeigte, dass die CDR in der ersten Runde mittels DBT erhöht war, in der folgenden Screening-Runde mit DM dann aber weniger Karzinome in diesem Arm zu finden waren – ein Hinweis darauf, dass durch die DBT Karzinome tatsächlich früher erkannt werden [13].
Empfehlungen zur DBT
Die European Commission Initiative on Breast Cancer schlägt daher vor, die DBT als Standard im Rahmen organisierter Screeningprogramme einzusetzen 14. Auch die AGO Kommission Mamma hält die Daten zur DBT in Kombination mit der SM im Rahmen der Früherkennung für ausreichend, um sie als Alternative zur DM zu empfehlen (LoE 1aA AGO+) [4].
Strahlenbelastung bei DBT
Bezüglich der Strahlenbelastung gibt es unterschiedliche Einschätzungen:
- In der norwegischen prospektiven Studie (To-Be Trial) führte die DBT/SM allein zu keiner zusätzlichen Strahlenbelastung [15]
- Aus der deutschen TOSYMA-Studie ergab sich bei weniger dichtem Drüsengewebe (BI-RADS A, B) eine mittlere Dosis für den Drüsenkörper bei DBT/SM etwa 48% höher als bei DM
- Bei dichtem Drüsengeweben (BI-RADS c, D) lag die Steigerung nur bei 27% bei gleichzeitig deutlicher Verbesserung der iCDR (invasive cancer detection rate)
- Bei einem BI-RADS Dichteindex von B, C, D lag die iCDR mit DBT allerdings nahezu doppelt so hoch wie mit DM
Mit der Einschränkung, dass es sich hier nur um explorative Ergebnisse handelt, schließen die Autoren, dass das Verhältnis von Benefit und Risiken für den Einsatz von DBT+SM bei Frauen mit dichtem Brustdrüsengewebe spricht 16. Offensichtlich ist, dass die Kombination von DBT und DM zu mehr als einer Verdoppelung der Strahlenbelastung führt, weshalb dieses Vorgehen zugunsten DBT/SM vermieden werden sollte. Alle Verfahren und Kombinationen liegen unter dem von der FDA empfohlenen Grenzwerten [5].
Abklärungsdiagnostik
Zur Abklärung auffälliger Befunde stehen klinische Untersuchung, die Mamma-Sonographie, Zusatzaufnahmen wie Spot-Kompression oder Vergrößerung, die DBT, die Kontrastmittel-gestützte Mammographie (CEM) und die MRT zur Verfügung. In Zweifelsfällen ist die Bildgebungs-gestützte Probengewinnung durch Stanzbiopsie (CNB) oder Vakuumbiopsie (VAB) Standard.
| Art der Bildgebung | Sensitivität | Spezifizität |
| Digitale Mammographie (DM) | 85 (78-90) | 77 (66-85) |
| Digitale Brust Tomosynthese (DBT) | 91 (87-94) | 85 (75-91) |
| Mamma-Sonographie | 90 (86-93) | 65 (46-80) |
| Kontrastmittel-verstärkte Mammographie (CEM) | 95 (90-97) | 73 (63-81) |
| Magnetresonanz-Tomographie (MRT) | 93 (88-96) | 69 (55-81) |
Kontrastmittel-verstärkte Mammographie (CEM)
Bei der CEM werden DM-Bilder mit unterschiedlichen low energy und high energy Spektren der Röntgenstrahlen (oberhalb und unterhalb der Absorptions-Kante von Jod) nach intravenöser Kontrastmittelgabe durchgeführt. Man erhält eine normale Mammographie sowie eine Subtraktionsaufnahme, die den Herd mit erhöhter Anreicherung zeigt. Kontrastmittel-speichernde Befunde infolge Kontrastmittel-Extravasation in den interstitiellen Raum, verstärkter Perfusion oder Gefäßdichte heben sich dann hervor (ähnlich wie bei der MRT). (Abb. 1)
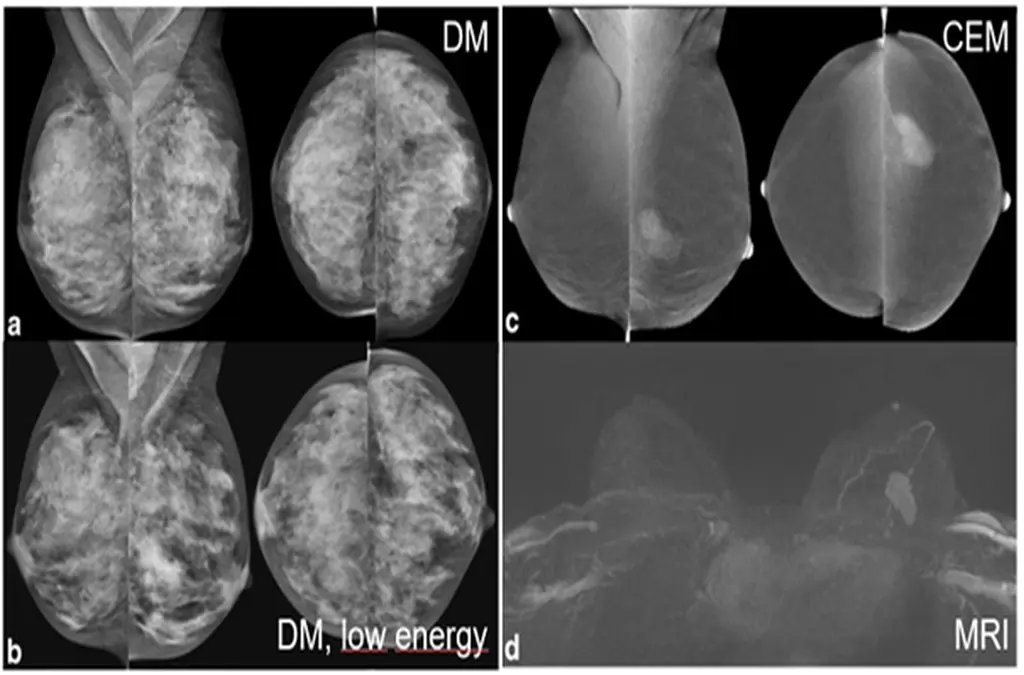
Studienergebnisse zur CEM
Gemäß einer 2024 publizierten Metaanalyse waren CEM, MRI, DBT und Mammasonographie geeignet, um Läsionen korrekt zu identifizieren und Karzinome korrekt zu klassifizieren; CEM und MRT übertreffen aber DM, DBT und Mammasonographie in den Parametern Sensitivität und Spezifität in der Abklärungsdiagnostik (Tabelle 1) [17].
In einer britischen prospektiven Studie (BRAID) wurden 9.361 Frauen mit dichtem Brustgewebe (BI-RADS Dichte-Grad C oder D) randomisiert einer Zusatzdiagnostik mit automatisiertem Ultraschall (ABUS), MRT oder CEM oder DM zugeführt [18]:
- Die CDR (invasiv und DCIS) mittels MRT war 17,4 (95% CI 12,2–23,9) auf 1.000 Untersuchungen
- Mittels CEM 19,2 (13,7–26,1)
- Mittels ABUS 4,2 (1,9–8,0)
- Die meisten der entdeckten Läsionen waren invasive Karzinome (85,9%)
- Der Unterschied zu ABUS war signifikant, kein Unterschied fand sich zwischen CEM und MRT
Für die Abklärungsdiagnostik werden daher heute CEM (LoE 1bB AGO+) und MRT (AGO 2aB +) als gleichwertige Alternativen empfohlen. Nachteil der CEM ist die geringe zusätzliche Strahlenbelastung. Eine MRT der Mammae sollte nur durchgeführt werden, wenn auch die Möglichkeit der MRT-gestützten Stanzbiopsie vorhanden ist.
Magnetresonanztomographie (MRT, MRI)
Die Magnetresonanztomographie hat ihren Stellenwert in der Abklärungsdiagnostik. Insbesondere bei dichtem Brustdrüsengewebe kann durch die MRT die CDR erheblich verbessert werden. Ergebnisse einer niederländischen prospektiven Studie (DENSE) zeigten, dass mittels MRT auch die Rate an Intervallkarzinomen bei Frauen mit sehr dichtem Brustgewebe signifikant gesenkt werden kann (von 5/1000 auf 0,8/1000 in einem 2-Jahresintervall) [19].
Neu sind sogenannte Abbreviated-MRI-Protokolle (Abb-MRI) mit einer Aufnahmezeit von [15] Minuten, mit denen ähnliche Ergebnisse wie mit der konventionellen-MRT erreicht werden, so dass sich diese für die Zukunft als Standard anbietet [20, 21].
Künstliche Intelligenz (AI)
In einer Re-Analyse zweier großer Datensätze des Mammographie-Screenings (UK, USA) konnte gezeigt werden, dass die AI ähnliche Ergebnisse liefert wie der Zweitbefunder und die Konsensuskonferenz und dabei die Arbeitsbelastung des Zweitbefunders um 88% reduzieren kann (Zweitbefundung nur bei unterschiedlichen Ergebnissen zwischen Erstbefunder und AI) [22]. Soweit erschien die AI ein vielversprechender Ansatz zu sein.
Eine kürzlich erschienene Metaanalyse zeigt dagegen, dass sich die CDR durch Einsatz von AI zur Zweitbeurteilung der Screening-Mammographie im Vergleich zur Befundung durch Radiologen nicht unterscheidet. Die Reduktion der Arbeitsbelastung des Zweitbefunders (hier ca. 50%) hängt dabei sehr von dem gewählten Studiendesign (inkl. Schwellenwerte und ggf. Drittbefundung) und der genutzten Bildgebung (DBT/SM, DM) ab und unterliegt daher einer hohen Variationsbreite [23].
AI zur Risikoidentifikation
Ein anderer Weg wird begangen, indem man die AI zur Identifikation von Frauen mit erhöhtem Risiko für falsch-negative Mammographien und Intervallkarzinome nutzt. Traditionell wird die dichte Brust als Risikofaktor angesehen. Eine höhere prognostische Aussagekraft wird AI-Algorithmen zugeschrieben, die auf der AI-gestützten Auswertung von Screening-Mammographien basieren.
Am Karolinska Institut in Stockholm wurden Frauen mit negativer Screening-Mammographie für eine prospektive Studie rekrutiert, in der eine zusätzliche MRT durchgeführt wurde, wenn aufgrund eines dort entwickelten AI-Algorithmus ein erhöhtes Risiko für falsch-negative Mammographien oder Intervallkarzinome vorlag:
- In dieser Kohorte wurde eine CDR von 64 Karzinomen pro 1.000 MRT-Untersuchungen beobachtet
- Als Vergleich wurden historische Daten herangezogen (DENSE-Trial); hier erfolgte bei extrem dichter Brust eine zusätzliche MRT
- Es ergab sich eine CDR von 16,5 pro 1.000 MRT [24]
Bewertung der AI in der Mammadiagnostik
Trotz vielversprechender Daten ist die Überlegenheit und Übertragbarkeit der AI in die Routine des Mammographie-Screenings nicht bewiesen, darüber hinaus fehlt auch die Standardisierung des Einsatzes von AI. Für den Ersatz für den Zweitbefunders sind die Daten nicht ausreichend. Es kann daher keine generelle Empfehlung zur Anwendung von AI in der Mammadiagnostik ausgesprochen werden (LoE 1bB AGO +/-) . Allenfalls zusätzlich zur Doppelbefundung kann AI möglicherweise zusätzliche Karzinome erkennen.
Neoadjuvante Therapie
Die Verlaufsbeurteilung unter neoadjuvanter Therapie erfolgt unverändert mit klinischer Untersuchung, Sonographie und Mammographie (LoE 2bB AGO ++); CEM und MRT sind als ergänzende Methode etabliert (LoE 2aB AGO +).
Schlussfolgerung
Das Mammographie-Screening ist eine Erfolgsgeschichte; in der Zielgruppe wird die Brustkrebs-spezifische Mortalität etwa um ein Drittel gesenkt. Das Programm bleibt ein lernendes System. Die Optimierung der Sensitivität, Spezifität, und die Senkung der Rate an Intervallkarzinom einerseits und der Rate überflüssiger Interventionen andererseits stehen im Zentrum der Entwicklung.
Mamma-Sonographie und MRT sind nach wie vor die Standardmethoden in der Abklärungsdiagnostik. Mit der Digitalen Brust-Tomosynthese, der Kontrastmittel-verstärkten Mammographie, der verkürzten Magnetresonanztomographie stehen schon heute verbesserte Verfahren zur Verfügung. Im Fokus der Forschung steht die Limitierung der Bildgebung bei dichtem Drüsenkörper. Vielleicht ist der Einsatz künstlicher Intelligenz der Weg, die Effektivität der Bildgebung hierbei zu verbessern.
Aus dem Heft onkologie heute 01/2026
Zur Literatur
Prof. Dr. Christoph Thomssen

Prof. Dr. Eva Maria Fallenberg



