Am Medias Klinikum wurde eine innovative Kombinationstherapie für Analkarzinome entwickelt, die gezielt und nebenwirkungsarm wirkt. In einer klinischen Fallserie erzielte die Methode – isolierte hypoxische Beckenperfusion gepaart mit reversibler Elektroporation – bei allen vier Patient*innen eine vollständige Tumorremission. Besonders bemerkenswert: Selbst Rückfälle nach erfolgloser Radiochemotherapie konnten organerhaltend behandelt werden.
Das Plattenepithelkarzinom des Anus betrifft jährlich etwa 2.500 Menschen in Deutschland und macht rund zwei Prozent aller gastrointestinalen Tumore aus. Die Standardtherapie mit Radiochemotherapie führt zwar in vielen Fällen zu guten Remissionsraten, verursacht jedoch erhebliche Nebenwirkungen wie Schleimhautentzündungen oder Hautreaktionen. Verschärfend kommt hinzu, dass bei Rückfällen oft nur eine Operation mit dauerhaftem künstlichem Darmausgang als Option bleibt.
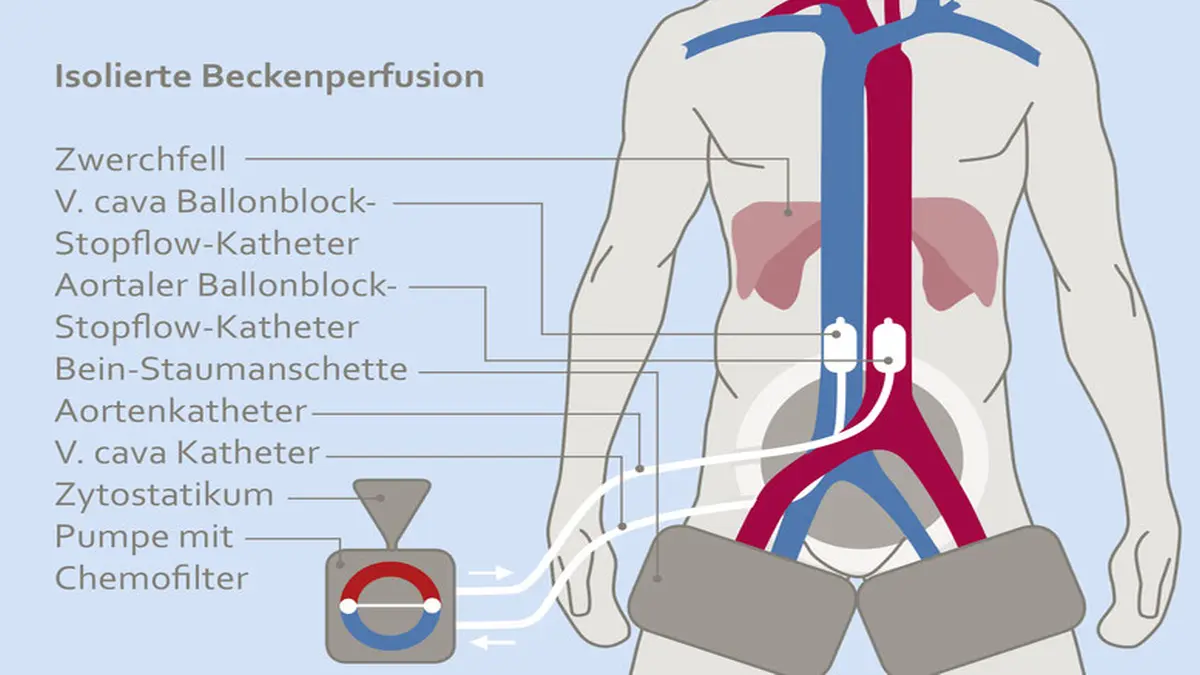
HPP: Präzise Wirkstoffverteilung durch isolierte Perfusion und Elektroporation
Das am Medias Klinikum entwickelte zweistufige Verfahren isoliert zunächst die Blutversorgung des Beckens durch strategisch platzierte Stop-Flow-Ballonkatheter vom allgemeinen Kreislauf. Über diese Katheter wird die Chemotherapie in rhythmischen Impulsen direkt in die Tumorregion geleitet. Durch die fünfminütige Unterbrechung des normalen Blutflusses entsteht eine hypoxische Perfusion im Becken. Dadurch können extrem hohe Wirkstoffkonzentrationen im Tumorbereich erzielt werden, die bei einer herkömmlichen Therapie nicht möglich wären.
Ergänzend kommt die reversible Elektroporation zum Einsatz: Über speziell platzierte Elektroden werden kurze elektrische Impulse abgegeben, die die Tumorzellen vorübergehend durchlässiger für die Chemotherapeutika machen. Die Medikamente werden gezielt während dieser elektrischen Impulse verabreicht, sodass sie noch effektiver in die Krebszellen eindringen können. Eine anschließende Chemofiltration entfernt überschüssige Zytostatika aus dem Blut und minimiert so die systemischen Nebenwirkungen für die Patient*innen.
Vollremission bei allen behandelten Patient*innen
Die Wirksamkeit dieser innovativen Methode wurde in einer klinischen Fallserie untersucht. Das Ärzteteam um Prof. Dr. Karl R. Aigner, Chefarzt und Ärztlicher Direktor am Medias Klinikum, behandelte vier Patient*innen mit HPV-positivem Analkrebs: Zwei primär unbehandelte G3-Karzinome (schlecht differenzierte, aggressive Tumore) erhielten eine isolierte Beckenperfusion und erreichten nach zwei bis drei Zyklen eine komplette klinisch-histologische Remission. Zwei rezidivierte G2-Karzinome (mäßig differenzierte Tumore) nach erfolgloser Radiochemotherapie wurden mit einer Kombination aus isolierter Beckenperfusion und Elektroporation (Elektrochemotherapie) behandelt und erreichten ebenfalls eine vollständige Tumorrückbildung.
Die dokumentierten krankheitsfreien Intervalle betrugen 8, 10, 27 und 48 Monate. Die Therapie verursachte keine schweren hämatologischen, gastrointestinalen oder dermatologischen Toxizitäten und es kam zu keiner therapiebedingten Einschränkung der Lebensqualität. Dies steht in deutlichem Kontrast zur konventionellen Radiochemotherapie, bei der die 5-Jahres-Überlebensrate zwischen 65 und 79 Prozent liegt und die teils mit erheblichen Spätfolgen einhergeht.
Anwendungsmöglichkeiten und Ausblick
Die Fallserie deutet darauf hin, dass die neue Kombinationstherapie eine wirksame und gleichzeitig schonendere Alternative zur etablierten Radiochemotherapie bei Analkarzinomen darstellen könnte. Besonders relevant ist die Methode für Patient*innen mit primären, lokal fortgeschrittenen Tumoren, therapieresistenten Karzinomen oder lokalen Rezidiven, bei denen bisher oft nur eine Operation mit dauerhaftem künstlichem Darmausgang infrage kam.
„Trotz der kleinen Kohorte sind die Ergebnisse sehr ermutigend. Die Fallserie wird aktuell fortgesetzt“, erklärt Prof. Dr. med. Karl R. Aigner, Ärztlicher Direktor und Chefarzt am Medias Klinikum. „Entscheidend ist für uns, dass wir Patient*innen eine organerhaltende Alternative anbieten können, die kaum Nebenwirkungen verursacht. Das ist ein großer Unterschied zur herkömmlichen Radiochemotherapie, bei der etwa die Hälfte der Patient*innen die Behandlung wegen der schweren Nebenwirkungen unterbrechen muss.“
Die isolierte hypoxische Beckenperfusion in Kombination mit Elektroporation ermöglicht eine hohe lokale Wirkstoffexposition bei minimaler systemischer Toxizität. Um die Wirksamkeit und Sicherheit dieser Methode im Vergleich zur etablierten Radiochemotherapie zu evaluieren, sind jedoch weitere prospektive Studien mit größeren Fallzahlen notwendig.
Quelle & Bildquelle: Pressemitteilung Medias Klinikum vom 25. September 2025