Das 5-Jahres-Überleben beim frühen, lokal begrenzten Mammakarzinom liegt heute bei über 90 %. Drei Haupttypen werden unterschieden: das Hormonrezeptor-positive, HER2-negative Mammakarzinom, das HER2-positive Mammakarzinom und das aggressive triple-negative Mammakarzinom mit der vergleichsweisen schlechtesten Prognose. Aktuell wird nach Biomarkern gesucht, die innerhalb dieser Gruppen eine weitere Differenzierung erlauben. Das Ziel ist, die Behandlung – zugeschnitten auf das individuelle Setting – so schonend wie möglich zu gestalten. Die Lebensqualität rückt dabei zunehmend in den Fokus. Strategien der Deeskalation werden geprüft und haben sich teilweise bereits etabliert. Andererseits sieht die zunehmend personalisierte Therapie bei hohem Rezidivrisiko eine Therapieeskalation vor. Der folgende Beitrag zur differenzierten Behandlung des frühen Mammakarzinoms folgt im Wesentlichen einer in „onkologie heute“ 8/2025 publizierten Übersicht [1].
HR-positives, HER2-negatives Mammakarzinom
Etwa 70 % aller Mammakarzinome weisen eine HR-positive, HER2-negative Tumorbiologie auf. Das heißt, Hormonrezeptoren – für Östrogen bzw. Progesteron – sind auf den Tumorzellen exprimiert. Die Prognose ist meist günstig (Luminal A), aber es gibt auch aggressivere Subtypen (Luminal B).
Standard beim frühen HR-positiven Mammakarzinom ist die adjuvante endokrine Therapie (AET). Laut einer retrospektiven Analyse profitieren auch Patientinnen mit sehr geringer HR-Expression (1–10 %) im Tumorgewebe von der AET. Die adjuvante endokrine Therapie sollte laut Empfehlung der AGO Kommission Mamma über mindestens fünf Jahre durchgeführt werden. In Abhängigkeit von Rezidivrisiko, Menopausenstatus und Verträglichkeit werden entweder der selektive Estrogen-Rezeptor-Modulator Tamoxifen oder ein Aromatase-Hemmer wie Anastrozol, Letrozol oder Exemestan eingesetzt. In der Prämenopause muss beim Einsatz von Aromatase-Hemmern gleichzeitig eine ovarielle Funktionssuppression erfolgen, um Wirkverluste und ausgeprägte Nebenwirkungen infolge gonadotroper Überstimulation zu vermeiden.
Genexpressionstest zur Risikospezifizierung
Die Indikation für oder gegen eine Chemotherapie ist beim frühen HR-positiven, HER2-negativen Mammakarzinom oft nicht eindeutig. Bei unklarer Indikation empfiehlt die AGO Kommission Mamma eine Genexpressionsanalyse an therapienaivem Tumorgewebe. Geeignete Gentests sind Oncotype DX, Mamma-Print und Endopredict.
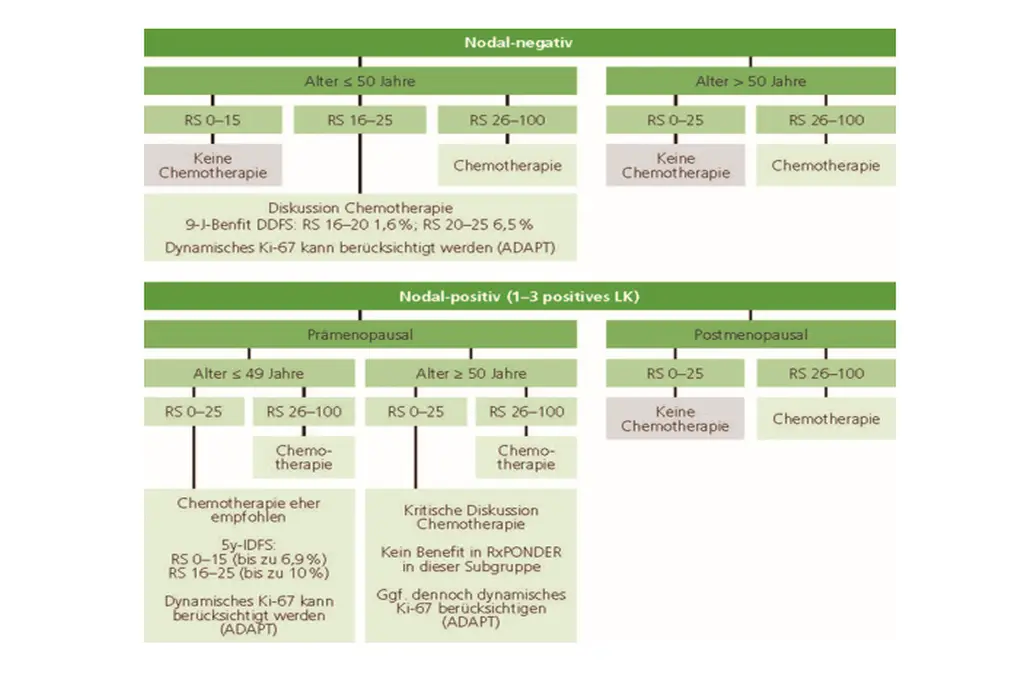
Mit dem Oncotype DX wird der Recurrence-Score (RS) ermittelt, der – basierend auf den prospektiven Studien TailorX und RxRsponder – Aussagen über den potenziellen Nutzen einer zusätzlich zur AET durchgeführten Chemotherapie erlaubt. In der TailorX-Studie wiesen 73 % der Patientinnen, die anhand klinischer Parameter als Hochrisikopatientinnen eingestuft wurden, einen niedrigen Oncotype DX RS (0–25) auf. Bei alleiniger Berücksichtigung des klinischen Risikos wären diese Patientinnen möglicherweise übertherapiert worden. Andererseits hatten 43 % der Patientinnen mit hohem RS ein niedriges klinisches Risiko und wären ohne die Genexpressionsanalyse eventuell unzureichend behandelt worden. Der Oncotype DX-Test kann inzwischen nicht nur bei nodal-negativen, sondern auch bei nodal-positiven Patientinnen als gesetzliche Kassenleistung abgerechnet werden.
Zusätzlich zur Genexpressionsanalyse kann eine endokrine Induktionstherapie für zwei bis vier Wochen durchgeführt werden. Vor und nach der Induktionstherapie wird der Proliferationsmarker Ki-67 bestimmt, um das sogenannte dynamische Ki-67 zu ermitteln. Ein deutlicher Abfall im Vergleich zum Vorwert auf ≤ 10 % kann als positiver Prädiktor für das Ansprechen auf die endokrine Therapie gewertet werden. Analog der ADAPT HR+/HER2– Studie kann bei intermediärem Oncotype DX RS (12–25) und maximal drei befallen Lymphknoten das dynamische Ki-67 als Entscheidungshilfe für einen möglichen Verzicht auf die Chemotherapie in der Prämenopause dienen.
Nachhaltiger Vorteil durch CDK4/6-Inhibitor
Patientinnen mit mittlerem bis hohem Rezidivrisiko können von einer kombinierten endokrinen Therapie profitieren, bei der zusätzlich der PARP-Inhibitor Olaparib oder ein CDK4/6-Inhibitor eingesetzt werden. Olaparib ist bei Nachweis einer pathogenen BRCA1/2– Keimbahnmutation indiziert und wird für ein Jahr zeitgleich mit der endokrinen Therapie gegeben. PARP-Inhibitoren blockieren die DNA-Reparaturmechanismen, was in Zellen mit homologer Rekombinationsdefizienz zu Doppelstrangbrüchen und anschließender Apoptose führt.
Eine weitere Option beim frühen HR-positiven, HER2-negativen Mammakarzinom sind die CDK4/6– Inhibitoren Abemaciclib und Ribociclib, die die Zellzyklusprogression hemmen. Ribociclib ist auch für Patientinnen ohne Nodalbefall mit intermediärem Risiko zugelassen. Die Neben- und Wechselwirkungsprofile der CDK4/6-Inhibitoren sind unterschiedlich, was bei der Therapieauswahl zu berücksichtigen ist.
In der NATALEE-Studie, einer randomisierten Phase-III-Studie, wurde gezeigt, dass Ribociclib das Überleben ohne invasive Krankheit (iDFS) nachhaltig günstig beeinflusst. [2] Eingeschlossen in die Studie wurden mehr als 5.000 Frauen mit HR+/HER2– Mammakarzinom Stadium I bis III und erhöhtem Rezidivrisiko. Ribociclib wurde zusätzlich zur endokrinen Standardtherapie mit einem nichtsteroidalen Aromatase-Hemmer gegeben, während die Kontrollgruppe einen Aromatase-Hemmer als Monotherapie erhielt. Die Ribociclib-Tagesdosis betrug 400 mg täglich, wobei nach 3 Wochen Therapie jeweils 1 Woche pausiert wurde. Die Behandlung wurde über drei Jahre durchgeführt. Die explorative Vier-Jahres-Analyse ergab einen langfristigen Benefit der Kombinationstherapie, der in allen Subgruppen – einschließlich nodal-negativer Patientinnen mit Risikofaktoren – in ähnlicher Größenordnung nachweisbar war. Die iDFS-Raten lagen bei 88,5 % versus 83,6 %. [3]
Die AGO Kommission Mamma empfiehlt Ribociclib zur adjuvanten Behandlung von prä-, peri- und postmenopausalen Frauen mit frühem HR+/HER2– Mammakarzinom in den Stadien II und III. Diese Empfehlung schließt auch Patientinnen mit einem Nodalstatus N0 ein, sofern Risikomerkmale vorliegen.
HER2-positives Mammakarzinom
Rund 15 % aller Mammakarzinome überexprimieren den humanen epidermalen Wachstumsfaktor-Rezeptor 2 (HER2). Bei grenzwertiger Immunhistochemie (ICH) erfolgt zusätzlich eine In-situ-Hybridisierung (ISH). HER2-positive Karzinome (IHC 3+/IHC 2+, ISH-positiv) sind in der Regel hochgradig chemosensibel.
Die hohe Wirksamkeit zielgerichteter Therapien, die den HER2-Rezptor adressieren, hat in der Behandlung des HER2-positiven Mammakarzinoms neue Perspektiven eröffnet. Um die Toxizität möglichst zu minimieren, wurde in diversen Studien geprüft, inwieweit man die neoadjuvante bzw. adjuvante Chemotherapie herunterfahren kann. Es hat sich gezeigt, dass dies in vielen Fällen möglich ist, ohne dass sich die Prognose verschlechtert. Es scheint sogar möglich, bei ausgewählten Patientinnen auf eine adjuvante Chemotherapie ganz zu verzichten.
Aktuelle Empfehlungen
Aktueller Standard beim frühen HER2-positiven Mammakarzinom ist eine neoadjuvante kombinierte Antikörper-Chemotherapie. Ausnahme sind nodal-negative Tumore von bis zu zwei Zentimetern, bei denen auf die neoadjuvante Therapie verzichtet wird. Nach der Operation erfolgt eine deeskalierte Systemtherapie über 12 Wochen mit Trastuzumab plus Paclitaxel (APT-Schema). Anschließend wird der Antikörper bei pathologischer Komplettremission (pCR) für ein Jahr als Monotherapie gegeben. Die 10-Jahres-Ergebnisse bei diesem Vorgehen sind überzeugend, die iDFS-Raten (invasives krankheitsfreies Überleben) lagen in der APT-Studie bei über 90 %. [4]
Bei größeren oder nodal-positiven Tumoren sind eine Polychemotherapie kombiniert mit einer dualen HER2-Blockade mit Trastuzumab und Pertuzumab zu bevorzugen. Bei unzureichendem Ansprechen auf die neoadjuvante Therapie im Sinne einer non-pCR empfiehlt die AGO die postneoadjuvante Eskalation auf das Antikörper-Wirkstoff-Konjugat Trastuzumab-Emtansin (T-DM1).
Neoadjuvante Therapie ohne Cisplatin
Weitere Studien sind unterwegs, die klären sollen, welche Patientinnen für verschiedene Deeskalationsstrategien in Frage kommen. Kürzlich wurden die Ergebnisse der neoCARHP-Studie publiziert, die zeigen, dass man im neoadjuvanten Setting auf das hochtoxische Cisplatin verzichten kann. [5] Eingeschlossen in die offene, randomisierte Phase-III-Studie wurden insgesamt 766 Patientinnen mit unbehandeltem HER2-positivem Mammakarzinom Stadium II bis III. Sie erhielten neoadjuvant ein Taxan plus Trastuzumab und Pertuzumab entweder in Kombination mit Cisplatin oder ohne Cisplatin (TCbHP versus THP). Mit Blick auf die Rate erzielter pathologischer Komplettremissionen war die platinfreie Therapie ebenbürtig bei deutlich geringerer Toxizität.
Komplettverzicht auf adjuvante Chemotherapie?
Eine weitere laufende Deeskalationsstudie – die Phase-II-Studie CompassHER2-pCR – prüft, ob bei Patientinnen mit frühem HER2-positivem Mammakarzinom, die nach einer verkürzten neoadjuvanten Therapie eine Komplettremission (pCR) erreichen, auf eine adjuvante Chemotherapie ganz verzichtet werden kann. Die verkürzte neoadjuvante Therapie bestand aus vier Zyklen Paclitaxel oder Docetaxel plus Trastuzumab und Pertuzumab (THP).
Bei 44 % der mehr als 2.000 Patientinnen konnte mit dem THP-Regime eine pathologische Komplettremission erzielt werden. In der Subgruppe mit HER2-positiven, Östrogenrezeptor-negativen Tumoren (HER2+ ER-) lag die Rate bei 63,7 %, bei HER2+ ER+ Tumoren waren es 32,4 %. Der HER2DX pCR Score erwies sich – unabhängig vom ER-Status – als valider Prädiktor für das Erreichen einer pathologischen Komplettremission. [6]
Patientinnen mit pCR erhalten im weiteren Verlauf der Studie keine adjuvante Chemotherapie, sondern ausschließlich eine duale HER2-Blockade mit Trastuzumab und Pertuzumab über ein Jahr. Primärer Endpunkt ist das rezidivfreie nach 3 Jahren. Die Daten werden Ende 2026 erwartet. Anschließend ist eine Nachbeobachtung über mehr als zehn Jahre vorgesehen.
Trastuzmab-Wirkstoff-Konjugate
Ein weiterer Ansatz, der helfen könnte, in Zukunft bei ausgewählten Patientinnen auf eine konventionelle systemische Chemotherapie zu verzichten, sind Antikörper-Wirkstoff-Konjugaten (ADCs) wie Trastuzumab-Emtansin (T-DM1) und Trastuzumab Deruxtecan (T-DXd). ADCs sind monoklonale Antikörper, an die über einen Linker ein zytotoxischer Wirkstoff (Payload) gekoppelt ist. Dieser wird durch den Antikörper zum antigen-tragenden Tumorgewebe transportiert und entfaltet dort – nach Lösung des Linkers – seine maximale Wirksamkeit.
T-DM1, das seit 2019 für die adjuvante Therapie des frühen HER2-positiven Mammakarzinoms zugelassen ist, besteht aus dem Antikörper Trastuzumab und dem Mikrotubuli-Inhibitor Emtansin. In der KATHERINE-Studie wurden Vorteile der T-DM1-Therapie gegenüber klassischem Trastuzumab mit Blick auf das Überleben ohne invasive Krankheit (HR 0,54) und das Gesamtüberleben (HR 0,66) nachgewiesen.
Mehrere Studien prüfen aktuell das Antikörper-Wirkstoff-Konjugat Trastuzumab-Deruxtecan (T-DXd) beim frühen HER2-positiven Mammakarzinom. Die randomisierte DESTINY-Breast 05 Studie vergleicht im non-pCR-Kollektiv den Einsatz von T-DXd mit T-DM1 (Head-to-Head Vergleich).
Weitere Antikörper-Wirkstoff-Konjugate befinden sich in der klinischen Entwicklung. Die verschiedenen ADC unterscheiden sich nicht nur hinsichtlich der Payload, sondern auch hinsichtlich des Bystander-Effekts, d.h. der Fähigkeit, auch antigen-negative Zellen in heterogenen Tumoren zu schädigen.
Triple-negatives Mammakarzinom
Das triple-negative Mammakarzinom (TNBC) macht rund 10 % aller Brustkrebserkrankungen aus. Aufgrund des aggressiven Wachstums und fehlender spezifischer Angriffspunkte auf der Tumoroberfläche ist die Prognose vergleichsweise ungünstig.
Aufgrund der oft hohen Proliferationsrate spricht das TNBC in der Regel jedoch gut auf eine Chemotherapie an. Die neoadjuvante Polychemotherapie ist Standard. Ausnahme sind sehr kleine, nodal-negative Tumore, bei denen die Chemotherapie nach aktueller Studienlage keinen zusätzlichen Nutzen bringt. Bei bestehender Indikation zur neoadjuvanten bzw. adjuvanten Chemotherapie sind platinhaltige Regime zu bevorzugen.
Für triple-negative Tumoren größer als zwei Zentimeter oder mit Nodalbefall ist seit 2022 der Immun-Checkpoint-Inhibitor (ICI) Pembrolizumab zugelassen. Dieser wird neoadjuvant gemeinsam mit der Chemotherapie verabreicht und postoperativ auf ein Jahr komplettiert. Überlebensdaten der Zulassungsstudie KEYNOTE-522 belegen einen signifikanten nachhaltigen Nutzen von Pembrolizumab auch im frühen Stadium unabhängig vom PD-L1-Status.
Auf BRCA1/2-Mutationen testen
Sind nach neoadjuvanter Therapie noch lokale oder axilläre Residuen nachweisbar, ist die Prognose schlecht. Risikoadaptiert wird die Therapie postneoadjuvant eskaliert. Wichtig ist die Testung auf BRCA1/2-Mutationen, die beim triple-negativen Brustkrebs häufig vorkommen. Bei positivem Testergebnis ist eine zielgerichtete Therapie mit dem PARP-Inhibitor Olaparib angezeigt. Eine weitere Option ist Capecitabin, ein oral verabreichtes Prodrug von 5-Fluoururacil. Zur Frage, ob Pembrolizumab postneoadjuvant mit Capecitabin oder Olaparib kombiniert werden sollte, liegen aktuell keine belastbaren Daten vor.
Fazit
- Angesichts sehr guter Überlebensdaten rückt bei der Behandlung des frühen Mammakarzinoms die Lebensqualität zunehmend in den Fokus. Es wird angestrebt, die Behandlung – je nach individueller Risikokonstellation – zu deeskalieren. Bei Hochrisiko-Patientinnen wird die Therapie gezielt eskaliert.
- Innovative Medikamente eröffnen die Möglichkeit, mit Blick auf die Toxizität den Einsatz konventioneller Chemotherapien herunterzufahren. Das gilt insbesondere für das HER2-positive Mammakarzinom.
- Beim HER2-positiven Mammakarzinom haben zielgerichtete Antikörper bzw. Antikörper-Wirkstoff-Konjugate die Behandlung revolutioniert.
- Beim HR-positiven, HER2-negativen Mammakarzinom mit hohem Rezidivrisiko haben sich die CDK4/6-Inhibitoren Abemaciclib und Ribociclib im adjuvanten Setting etabliert.
- Aufgrund des aggressiven Wachstums und fehlender spezifischer Angriffspunkte auf der Tumoroberfläche ist die Prognose des triple-negativen vergleichsweise ungünstig. Das betrifft insbesondere Patientinnen, die nach neodjuvanter Chemotherapie keine pathologische Komplettremission erreichen.
- Die neoadjuvante – bevorzugt platinhaltige – Polychemotherapie ist Standard.
- Als innovative Wirkstoffe stehen für die Behandlung des triple-negtiven Mammakarzinoms der Immun-Checkpoint-Inhibitor Pembrolizumab sowie der PARP-Inhibitor Olaparib zur Verfügung, der bei Patientinnen mit BRCA1/2-Mutationen zum Einsatz kommt. Angesichts der Häufigkeit von BRCA1/2-Mutationen sollten alle Patientinnen mit TNBC molekulargenetisch getestet werden.
Ulrike Viegener



