Wie lassen sich Patienten mit Prostatakarzinom vor Übertherapie schützen, ohne das Risiko einer Tumorprogression zu erhöhen? Der folgende Artikel beleuchtet aktuelle Empfehlungen und neue Entwicklungen zur Aktiven Überwachung – inklusive moderner Diagnostik und differenzierter Patientenselektion. Für wen ist dieses Vorgehen geeignet und welche Herausforderungen und Chancen bietet die Active Surveillance im klinischen Alltag?
Bei der Diagnosestellung eines Prostatakarzinoms (PCa) erfolgt eine klinische Risikoeinteilung der Patienten in eine Gruppe mit einem niedrigen, mittleren (intermediären) oder hohen Risiko für eine Tumorprogression und krankheitsspezifische Mortalität [1]. Ein PCa der niedrigen und mittleren Risikogruppe führt nur bei wenigen Betroffenen zum tumorbedingten Tod [2 – 4].
Aufgrund der Nebenwirkungen von Lokaltherapien stellt die Aktive Überwachung (Active Surveillance; AS) eine attraktive Option dar, um eine Übertherapie zu vermeiden. Die AS wird bei geeigneten Patienten angewendet und zielt darauf ab, eine Lokaltherapie zunächst zurückzustellen und nur im Falle einer tatsächlichen Tumorprogression eine kurative Therapie durchzuführen.
Patienten mit einem Prostatakarzinom der niedrigen Risikogruppe (ISUP 1 und low-risk nach d’Amico) sollen aktiv überwacht werden. Patienten mit einem Prostatakarzinom der mittleren Risikogruppe und gleichzeitig günstigen Prognosekriterien (ISUP 2, d. h. Gleason-Score 7a (3 + 4) mit sehr geringem Anteil eines Gleason 4-Musters in der Biopsie ohne intraduktales oder cribriformes Tumorwachstum) können ebenfalls aktiv überwacht werden.
(Kontra-)Indikationen zur Active Surveillance
Für die AS kommen Patienten mit einem niedrigen Risiko nach d’Amico in Frage. Bei der Diagnostik des PCa wird immer häufiger eine MRT und nachfolgend eine zielgerichtete Prostatabiopsie von auffälligen MRT-Arealen, eine sog. MRT-TRUS-Fusionsbiopsie, durchgeführt.
Dadurch haben sich die Einschlusskriterien für eine AS beispielsweise bezüglich der „Anzahl der befallenen Stanzzylinder” und dem „Karzinomanteil in einem Stanzzylinder” verändert [5]. Folglich spielt bei vorliegender MRT die digital-rektale Untersuchung für die Entscheidung für oder gegen eine AS nur noch eine nachrangige Rolle.
Bei lokal begrenztem PCa der Niedrigrisiko-Gruppe sollte nur eine AS erfolgen, da hier das Risiko einer Überbehandlung am höchsten ist. Das niedrige Risiko wird nach den ISUP-Kriterien bestimmt. Alternativ wird auch die d’Amico-Klassifikation genutzt, die jedoch zunehmend durch die Leitlinien des National Comprehensive Cancer Network (NCCN) ersetzt wird.
Die Empfehlung basiert auf den Daten einer großen prospektiven Studie bei Niedrigrisiko-PCa. Es zeigte sich nach 15 Jahren eine PCa-spezifische Mortalität von < 1 % unter AS [6]. Patienten, deren initiale Diagnostik eine MRT / TRUS-fusionierte Prostatabiopsie beinhaltete, hatten ein geringeres Risiko für eine Reklassifikation während der AS und damit für die Notwendigkeit einer aktiven Therapie im weiteren Verlauf (ca. 50 % der Patienten mussten sich doch einer Therapie unterziehen).
Die AS-Strategie kann auch bei Patienten mit intermediärem Risikoprofil in Betracht gezogen werden. In der viel beachteten PROTECT-Studie wurden 1.643 Männer mit lokalisiertem PCa in die Behandlungsgruppen „Aktives Monitoring”, radikale Prostatektomie und externe Radiotherapie randomisiert. 34 % der Patienten hatten ein intermediäres oder sogar hohes Risiko [7, 8].
Die krankheitsspezifische Mortalität war in allen Gruppen gleich niedrig, jedoch war „Aktives Monitoring” mit einem höheren Progressionsrisiko assoziiert. Insbesondere Patienten mit einem intermediären Risikoprofil haben ein höheres Risiko für eine Progression und Metastasierung als Patienten in der Low-Risk-Gruppe [9, 10]. Studien zeigen, dass AS für einige Patienten mit intermediärem Risiko geeignet erscheint, wenn ein günstiges Risikoprofil vorliegt (kein cribriformes oder intraduktales Wachstum, geringer Anteil von Gleason-Muster 4) [5, 11].
Patienten mit PCa des ISUP-Grades 3 oder mit intraduktaler oder cribriformer Histologie, also biologisch aggressiven Tumoren, sollten nicht für AS in Betracht gezogen werden. Ein höherer Anteil von Gleason Muster 4 ist mit einem deutlich erhöhten Rezidivrisiko verbunden [12, 13].
Die Festlegung eines PSA-Schwellenwertes für die AS wird in den Leitlinien kontrovers diskutiert, da größere Prostatadrüsen höhere PSA-Werte verursachen können. Diese Einzelfälle sind in der Leitlinie nicht berücksichtigt. Ein Schwellenwert von ≥ 15 ng / ml erscheint gegenüber der Grenze von 10 ng / ml in den d’Amico-Kriterien als praktikabler.
In der prospektiven Studie von Klotz und der PROTECT-Studie wurden Patienten mit PSA-Werten bis < 20 ng/ml eingeschlossen [7,14]. Eine AS bei Patienten mit PSA-Werten bis 15 ng / ml ist vertretbar, wenn die weiteren Einschlusskriterien und die MRT-Darstellung auf ein niedriges Risiko hinweisen. Zusätzlich kann die PSA-Dichte (PSA-D) hilfreich sein; sie berechnet sich aus dem Quotienten PSA im Blut (in ng / ml) geteilt durch das Volumen der Prostata (in ml), ein Wert > 0,3 ist stark mit einem klinisch signifikanten Prostatakarzinom verbunden.
Praktische Durchführung der Active Surveillance
Die AS setzt einen engen Patientenkontakt und eine sorgfältige Tumorkontrolle voraus, um Übertherapien zu vermeiden und gleichzeitig eine Tumorprogression frühzeitig zu erkennen. Ziel ist es, Nebenwirkungen aktiver lokaler Therapien (OP oder Strahlentherapie) zu vermeiden, ohne dabei die Chance auf Heilung bei Progression zu gefährden.
Studien zeigen, dass 30–61 % der Patienten im Verlauf von AS in eine aktive Therapie überführt werden; bei bis zu 17 % geschieht dies ohne Progressionszeichen, allein auf Wunsch der Patienten [8, 15–17]. In der PROTECT-Studie lebten zuletzt 24,4 % der Männer ohne jegliche Therapie, bei Patienten mit initial intermediärem oder hohem Risiko waren es nur 12,8 % [8].
Aktuelle Empfehlungen lösen sich von strikt dreimonatlichen Kontrollen des PSA-Wertes. In der PROTECT-Studie erfolgten PSA-Messungen im ersten Jahr vierteljährlich, danach halbjährlich bis jährlich [7]. Ähnlich wurde in der PRIAS-Studie verfahren; dort stiegen 41 % der Patienten innerhalb von 10 Jahren wegen histologischer Progression auf eine aktive Therapie um [18].
Die Studie DETECTIVE empfiehlt mindestens halbjährliche PSA-Kontrollen zur Beurteilung von PSA-Verdopplungszeit und -dichte, beides relevante Parameter zur Progressionseinschätzung [5].
Erneute Biopsien (als 1. Re- bzw. konfirmatorische Biopsie) dienen der Bestätigung der initialen Diagnose und der Detektion histologischer Progression. Der Zeitpunkt hängt von der Qualität der Erstdiagnostik ab.
Eine Active Surveillance soll nicht durchgeführt werden bei:
- initialem PSA-Wert ≥ 15 ng / ml
- ISUP-Gruppe 2 mit ungünstigen Kriterien
Hochrisiko-Prostatakarzinom
Nach initialer mpMRT und gezielter Biopsie wird eine Wiederholung nach 12 – 18 Monaten empfohlen [19]. Bei fehlender mpMRT sollte innerhalb von sechs Monaten eine kombinierte (mpMRT / TRUS-fusionierte und systematische) Biopsie erfolgen.
Kombinierte Verfahren verbessern die Erkennung signifikanter Tumoren und senken die Rate an Therapieabbrüchen während der AS [20]. Systematische Biopsien behalten ihre Relevanz – insbesondere, um Zielverfehlungen bei alleiniger Target-Biopsie zu vermeiden und die diagnostische Sicherheit zu erhöhen.
Repetitive MRT-Bildgebungen und Biopsien?
Wird bei der ersten Re-Biopsie keine Tumorprogression festgestellt, kann die AS fortgesetzt werden. Die optimalen Intervalle für PSA-Kontrollen, MRT-Bildgebung und Re-Biopsien sind bislang nicht eindeutig evidenzbasiert. Sowohl die EAU als auch die deutsche S3-Leitlinie empfehlen derzeit Re-Biopsien im Abstand von drei Jahren [5, 19, 21].
Die multiparametrische MRT (mp-MRT) bietet durch ihre hohe Sensitivität für signifikante Tumorveränderungen ein zunehmend wichtiges Werkzeug für das Monitoring unter AS [5, 22, 23]. Sie erlaubt eine morphologisch-funktionelle Darstellung der Prostata und ist Grundlage für die Anwendung des PRECISE-Score-Systems (Prostate Cancer Radiological Estimation of Change in Sequential Evaluation) (▶ Abb. 1) [7, 15]. Dieses bewertet sequentielle MRT-Verläufe standardisiert.
Die MRT-Bildgebung der Prostata gewinnt zunehmend an Bedeutung sowohl zur initialen Fusionsbiopsie und bestmöglichen Selektion von geeigneten Patienten für eine sichere Aktive Überwachung, als auch im Laufe der Aktiven Überwachung zur Kontrolle.
Der PRECISE-Score reicht von 1 (Regress) bis 5 (extrakapsuläre Ausdehnung, Samenblaseninfiltration, Metastasen). Version 2 differenziert PRECISE 3 in stabile Läsionen (3-V) und unspezifische diffuse Veränderungen (3-NonV). Eine Zunahme der Läsion ≥ 50 % (PRECISE 4) oder Hinweise auf lokoregionäre Ausbreitung (PRECISE 5) gelten als starker Hinweis auf Progression [24, 25].
Obwohl PRECISE-gesteuerte Re-Biopsien laut Daten zwei Drittel der Biopsien einsparen könnten, bleibt ein Restrisiko bestehen. Daher wird weiterhin empfohlen, innerhalb der ersten zehn Jahre der AS alle drei Jahre eine Re-Biopsie durchzuführen [5, 19, 26].
Die PROMM-AS-Studie zeigte, dass bei stabilem MRT (PRECISE ≤ 3) die Biopsie um ein Jahr verschoben werden konnte. Bei Progress (PRECISE ≥ 4) sollte sie hingegen umgehend erfolgen. Nach 24 Monaten konnten 88 % der Patienten mit ISUP Grad 1 und stabilem MRT eine Biopsie vermeiden, während bei MRT-Progress in 81 % korrekt ein Therapieabbruch empfohlen wurde [27].
Auch PSA-Dichte (PSAD) und PSA-Dynamik fließen in die Entscheidung zur Re-Biopsie ein. Eine PSAD ≥ 0,2 gilt nach PRIAS als biopsiewürdig [2]. Ein PSA-Anstieg allein rechtfertigt jedoch keinen Abbruch der AS.
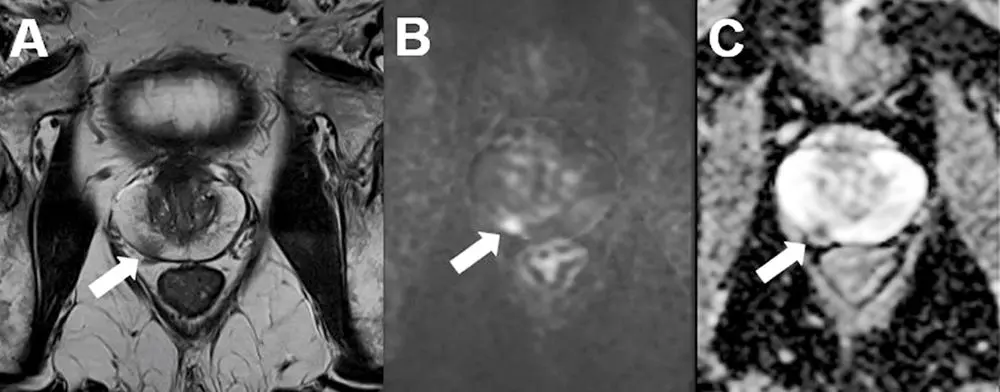
Axiale Schichtung einer mpMRT mit karzinomsuspektem Befund in der peripheren Zone rechts (PIRADS 4) in der T2-Sequenz (A) mit Nachweis einer Diffusionsstörung (B+C). Die daraufhin durchgeführte MRT-TRUS-Fusionsbiopsie der Prostata ergab ein Prostatakarzinom mit einem Gleason-Score 3 + 4 = 7a (Gleason 4-Anteil: 10 %). (mit freundlicher Genehmigung von Dr. med. Daniel Vogele, Klinik für Diagnostische und Interventionelle Radiologie, Universitätsklinikum Ulm)
Abbruchkriterien für eine Active Surveillance
Während der AS müssen Wohlbefinden und Wünsche des Patienten regelmäßig geprüft werden. Bis zu 10 % der Patienten entwickeln Ängste, die zu einem Therapiewechsel führen können. In der PRIAS-Studie wechselten 5 % aus Angst in eine aktive Therapie [18].
Neu auftretende Komorbiditäten mit potenzieller Lebenszeitverkürzung können zudem einen Strategiewechsel hin zum Watchful Waiting erforderlich machen. AS sollte nur fortgesetzt werden, wenn der Patient zustimmt, keine relevante Komorbidität hinzugekommen ist und keine Tumorprogression vorliegt.
Ein signifikanter PSA-Anstieg oder eine kurze PSA-Verdopplungszeit (< 3 Jahre) erfordern eine Re-Evaluation, sollten jedoch nicht isoliert zur Therapieeskalation führen, da der PSA-Wert von vielen Faktoren beeinflusst wird. Die Rolle der MRT gewinnt an Bedeutung. Laut DETECTIVE-Meeting rechtfertigen eine Zunahme der PIRADS-Klassifikation oder ein deutlicher PSA-Anstieg eine Re-Biopsie [5].
Auch die PSA-Dichte (PSAD) hat prognostische Relevanz: Eine PSAD ≥ 0,2 ist mit einem erhöhten Progressionsrisiko assoziiert [28, 29]. Daher sollte bei auffälligem PSA-Verlauf eine mp-MRT mit gezielter und systematischer Re-Biopsie erfolgen – eine reine PSA- oder MRT-Progression rechtfertigt jedoch keinen automatischen Abbruch der AS.
Fazit
Die Aktive Überwachung stellt ein onkologisch sicheres Verfahren dar für Patienten mit einem neu diagnostizierten Prostatakarzinom in der niedrigen Risikogruppe als auch für vorsichtig ausgewählte Patienten in der intermediären Risikogruppe.
Eine ausführliche Aufklärung und eine engmaschige konsequente Durchführung fachärztlicher Beratungen und Kontrolluntersuchungen sind integraler Bestandteil der Aktiven Überwachung.
Die erste Re-Biopsie der Prostata sollte 12 bis 18 Monate nach Beginn der Aktiven Überwachung erfolgen, um eine Tumorprogression auszuschließen. Eine frühere, innerhalb von sechs Monaten durchzuführende konfirmatorische Kontrolle durch MRT/TRUS-Fusionsbiopsie wird empfohlen, wenn die initiale Diagnose mittels konventioneller Biopsie gestellt wurde.
Die Entscheidung für weitere Biopsien im Rahmen einer fortgesetzten Aktiven Überwachung kann zunehmend durch bildgebende Verlaufskontrollen mittels Prostata-MRT, vorzugsweise unter den gleichen technischen Bedingungen wie bei der Voruntersuchung und unter Anwendung der PRECISE-Empfehlungen getroffen werden.
Ein alleiniger Anstieg des PSA-Wertes oder eine bildmorphologische Progression in der MRT sind keine ausreichenden Indikatoren für den Beginn einer aktiven Therapie, sondern können zunächst die Notwendigkeit für eine Re-Biopsie triggern. Priorität hat zu jedem Zeitpunkt während der Aktiven Überwachung jedoch ein möglicherweise aufkommender Patientenwunsch nach einer aktiven Therapie.
Folgende Kriterien führen zum Abbruch der aktiven Überwachung und zur Initiierung einer aktiven Therapie oder zum Wechsel in Watchful Waiting:
- Wunsch des Patienten nach Änderung des Konzeptes (z. B. aus Angst)
- Upgrading zur ISUP-Gruppe 2 mit ungünstigem Risikoprofil (cribriformes oder intraduktales Wachstum, höherer Anteil Gleason-Muster 4)
- Upgrading zu ISUP-Gruppe 3 oder höher
- Auftreten eines lokal fortgeschrittenen Tumorstadiums (≥ cT3 und/oder cN+)
Prof. Dr. Christian Bolenz
Interessenkonflikte:
F. Zengerling hat Berater- und Referentenhonorare sowie Reisekostenunterstützung von Amgen, Apogepha, Astellas, AstraZeneca, Bayer Health, BMS, Daiichi Sankyo, Ipsen, Janssen-Cilag, Johnson& Johnson, Merck, MSD, Novartis, Onkowissen, Pfizer, Roche sowie Sanofi/Aventis erhalten.
C. Bolenz ist Mitglied der Leitliniengruppe zur Erstellung der S3-Leitlinie Prostatakarzinom im Rahmen des Leitlinienprogrammes Onkologie der Deutschen Krebsgesellschaft, der Deutschen Krebshilfe und der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF). CB ist Vorstandsmitglied der Deutschen Gesellschaft für Urologie (Ressort Haushalt und Finanzen). Berater- und Referentenhonorare sowie Reisekostenunterstützung wurden von AstraZeneca, Bayer, BMS, Johnson& Johnson, Ferring sowie Cepheid erhalten
Literatur unter www.uroforum.de