Die Systemtherapie des Prostatakarzinoms hat sich in den vergangenen Jahren deutlich gewandelt. Molekulare Kartierungs- und Sequenzierungsprogramme haben eine ausgeprägte biologische Heterogenität, insbesondere im metastasierten Stadium, aufgezeigt und damit die Grundlage für personalisierte Therapiekonzepte geschaffen. Dieser Review gibt einen Überblick über zentrale molekulare Alterationen und therapeutisch relevante Abhängigkeiten, darunter Defekte der homologen Rekombinationsreparatur, Veränderungen des PTEN / PI3K / AKT-Signalwegs sowie molekulare Korrelate aggressiver Tumorbiologien. Darüber hinaus werden zielgerichtete Therapien gegen tumorassoziierte Zelloberflächenproteine, einschließlich Radioligandentherapien, Antikörper-Wirkstoff-Konjugaten und T-Zell-Engagern, zusammenfassend dargestellt. Perspektivisch eröffnen integrierte molekulare und funktionelle Diagnostik sowie adaptive Therapiestrategien die Chance, Behandlungsentscheidungen zunehmend dynamisch und präzise an die individuelle Tumorbiologie anzupassen.
Hintergrund
Über viele Jahre war die Systemtherapie des Prostatakarzinoms – insbesondere im fortgeschrittenen Stadium – durch relativ uniforme Behandlungspfade geprägt und folgte damit einer „one size fits all”-Strategie: Androgendeprivationstherapie (ADT) als Basis, darauf aufbauend eine Sequenz aus Androgenrezeptor-gerichteten Substanzen und Taxanen.
Große molekulare Kartierungsprojekte und klinische Sequenzierungsprogramme haben gezeigt, dass Prostatakarzinome biologisch hoch heterogen sind – sowohl im Primärtumor als auch (und besonders) in der metastasierten, kastrationsresistenten Situation. Bereits eine TCGA (The Cancer Genome Atlas)-Analyse primärer Prostatakarzinome definierte eine molekulare Taxonomie mit molekularen Treibern und unterstrich damit, dass das Prostatakarzinom kein einheitliches Krankheitsbild darstellt, sondern ein Spektrum unterschiedlicher Subtypen mit potenziell divergierenden Vulnerabilitäten 1.
Prospektive, multizentrische Sequenzierungsprogramme identifizierten bei Patienten mit metastasierten, kastrationsresistenten Prostatakarzinomen (mCRPC) eine Anreicherung mutmaßlich therapiegetriebener Veränderungen (u. a. AR-Aberrationen, TP53 / PTEN-Veränderungen) und etablierten damit den präzisionsonkologischen Rahmen, der heute zunehmend die Therapieplanung mitbestimmt 2.
Auf dieser biologischen Grundlage wurde die Personalisierung der Therapie klinisch greifbar. Dazu zählen u. a. die therapeutische Nutzbarmachung von alterierten Signaltransduktionswegen und Defekten der DNA-Reparatur sowie tumorzelluläre Oberflächenstrukturen als Targets („Surfaceome”).
Schließlich hat auch das Immunsystem – trotz der insgesamt als eher „immunologisch kalt” beschriebenen Biologie vieler Prostatakarzinome – einen zunehmend definierten Stellenwert im Kontext individualisierter Therapiekonzepte erlangt.
Im Folgenden soll ein Einblick in die Entwicklung personalisierter Therapiekonzepte beim Prostatakarzinom geben werden. Anhand ausgewählter Beispiele werden aktuelle Entwicklungen und klinisch relevante Fortschritte dargestellt, zugleich werden bestehende Limitationen sowie zentrale Herausforderungen für die Implementierung individualisierter Therapieansätze im klinischen Alltag kritisch beleuchtet.
HRR-Defizienz und Wirkprinzip der PARP-Inhibition
Ein zentraler Baustein der personalisierten Therapie des fortgeschrittenen Prostatakarzinoms ist die Identifikation von Defekten in der homologen Rekombinationsreparatur (homologous recombination repair, HRR). Die HRR ist ein wichtiger Mechanismus zur präzisen Reparatur von DNA-Doppelstrangbrüchen.
Pathogene Alterationen in HRR-Genen – insbesondere BRCA1, BRCA2, aber auch ATM, PALB2, CHEK2 und weiteren Genen – führen zu einer eingeschränkten Reparaturkapazität und damit zu einer erhöhten genomischen Instabilität 2, 3.
Dabei ist das Auftreten von HRR-Alterationen von prognostischer Relevanz. Insbesondere BRCA1 / 2-Mutationen sind in fortgeschrittenen Krankheitsstadien mit einem ungünstigeren Verlauf assoziiert, einschließlich eines verkürzten progressionsfreien und Gesamtüberlebens. Aber auch nicht-BRCA-HRR-Alterationen gehen im Vergleich zu HRR-intakten Tumoren mit einer schlechteren Prognose einher, wenngleich weniger ausgeprägt.
Diese Zusammenhänge zeigen sich sowohl im kastrationsresistenten als auch bereits im hormonsensitiven metastasierten Stadium und unabhängig von der gewählten Systemtherapie (ARPI oder Taxane) 4, 5.
PARP-Inhibitoren blockieren die Reparatur von DNA-Einzelstrangbrüchen durch Hemmung der Poly(ADP-Ribose)-Polymerase. In HRR-defizienten Tumorzellen führt dies zu einer Akkumulation letaler DNA-Schäden („synthetische Letalität”), während gesunde Zellen mit intakter HRR diese Schäden kompensieren können 6.
Olaparib ist das erste Biomarker-basierte Medikament und gleichzeitig der einzige PARP-Inhibitor, der in Europa für die Monotherapie des mCRPC bei Vorliegen einer pathogenen BRCA1 / 2-Alteration zugelassen ist. Die Zulassung basiert auf der randomisierten Phase-III-Studie PROFOUND, in der Patienten mit einem nachgewiesenen HRR-Defekt und Vorbehandlung mit mindestens einer AR-gerichteten Therapie eingeschlossen wurden; eine vorherige Docetaxel-Therapie war erlaubt.
Die Patienten wurden nach Art der HRR-Alteration stratifiziert (Kohorte A: BRCA1 / 2 oder ATM, Kohorte B: andere HRR-Gene). Die Studie erreichte ihren primären Endpunkt mit einer signifikanten Verbesserung des radiographischen progressionsfreien Überlebens (rPFS) gegenüber der Therapie nach ärztlicher Wahl (Abirateron oder Enzalutamid). Auch das Gesamtüberleben war signifikant verlängert, wobei der Effekt weitestgehend durch Patienten mit BRCA1 / 2-Mutation getragen wurde 7.
Neben der Monotherapie hat sich die Kombination von PARP-Inhibitoren mit AR-gerichteten Therapien als wichtiger Entwicklungsschritt etabliert. PARP1 fungiert nicht nur als DNA-Reparaturenzym, sondern auch als Koaktivator des Androgenrezeptors (AR). Eine PARP-Inhibition kann daher die AR-Signalübertragung direkt abschwächen 8.
Zusätzlich führt die Hemmung des AR-Signalwegs zu einer verminderten Expression von HRR-Genen, wodurch ein funktioneller HRR-Defekt induziert wird und Tumorzellen stärker von PARP-vermittelter Reparatur abhängig werden 8.
Drei Phase-III-Studien untersuchten diese Strategie in der Erstlinie des mCRPC: PROPEL (Abirateron + Olaparib), TALAPRO-2 (Enzalutamid + Talazoparib) und MAGNITUDE (Abirateron + Niraparib) 9 – 11. Trotz ähnlicher Grundkonzepte unterscheiden sich die Studien im Design. Während PROPEL und TALAPRO-2 als „All-Comer-Studien” durchgeführt wurden, trennte MAGNITUDE die Patienten nach HRR-Status; der HRR-negative Arm wurde aufgrund fehlender Wirksamkeit frühzeitig gestoppt 12.
PROPEL und TALAPRO-2 zeigten eine signifikante Verbesserung des rPFS und eine bedeutsame Verlängerung in der Gesamtpopulation (mit signifikantem Überlebensvorteil für Enzalutamid / Talazoparib) im Vergleich zur alleinigen AR-gerichteten Therapie. MAGNITUDE bestätigte den Nutzen der Kombinationstherapie in der HRR-defizienten Population 9 – 11. Die Sensitivität gegenüber der Kombination aus PARP-Inhibitoren und AR-gerichteter Therapie war dabei wesentlich von der zugrunde liegenden HRR-Alteration abhängig.
Der größte und konsistenteste klinische Nutzen zeigte sich in einer Metaanalyse aller drei Studien bei BRCA2– und BRCA1-Mutationen, während kein Benefit bei ATM- und CHEK2-Alterationen nachgewiesen wurde. Eine vielversprechende Aktivität konnte dagegen bei den seltenen CDK12- und PALB2-Alterationen beobachtet werden 12.
Damit wird deutlich, dass trotz der „All-Comer”-Zulassung für die Kombinationen aus Abirateron / Olaparib sowie Talazoparib / Enzalutamid nicht alle Patienten in gleichem Maße von diesem Therapieansatz profitieren. Vielmehr ist eine individuelle Risiko-Nutzen-Abwägung erforderlich, die sich an der zugrunde liegenden HRR-Alteration, dem Nebenwirkungsprofil der Kombinationstherapie sowie dem physischen Zustand des Patienten orientiert.
Erste Daten zur PARP-Inhibitor- / ARPI-Kombination in der hormonsensitiven Situation zeigen, dass die Hinzunahme von Niraparib zu Abirateron / Prednison bei Patienten mit HRR-alteriertem mHSPC zu einer signifikanten Verlängerung des radiographischen progressionsfreien Überlebens sowie zu einer Verzögerung der symptomatischen Progression führt, wiederum mit dem größten Nutzen bei BRCA1 / 2-Alterationen 13.
Der PTEN/AKT-Signalweg
Der Tumorsuppressor Phosphatase and Tensin Homolog (PTEN) auf Chromosom 10 und die nachgeschaltete PI3K / AKT / mTOR-Signalkaskade zählen zu den am häufigsten veränderten molekularen Signalwegen des Prostatakarzinoms. PTEN fungiert als dual-spezifische Phosphatase und antagonisiert die PI3K-Signalgebung, indem es Phosphatidylinositol-3,4,5-trisphosphat (PIP3) zu Phosphatidylinositol-4,5-bisphosphat (PIP2) dephosphoryliert und damit die Aktivierung von AKT und mTOR hemmt.
Eine Inaktivierung von PTEN durch Deletion oder Mutation führt zu einer unkontrollierten AKT-Aktivierung mit konsekutiver Modulation zentraler zellulärer Prozesse, darunter Apoptose, Zellzyklusregulation, Proliferation, Metabolismus, Differenzierung und Invasivität 14, 15.
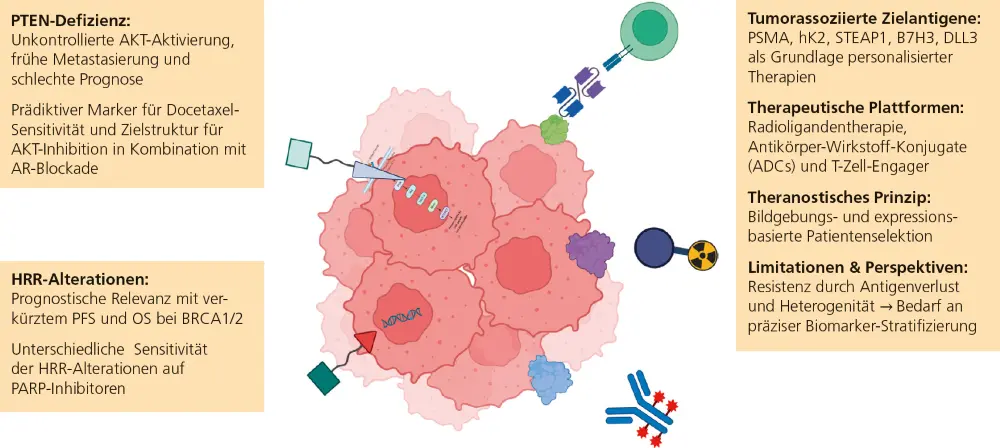
PTEN-Verlust ist beim Prostatakarzinom mit einem aggressiven klinischen Phänotyp assoziiert und korreliert mit höherem Tumorstadium, früher Metastasierung, androgenunabhängiger Tumorprogression sowie einer erhöhten prostatakarzinomspezifischen Mortalität 15. In Abhängigkeit vom Krankheitsstadium werden PTEN-Deletionen bei etwa 20 – 50 % der Patienten nachgewiesen.
Aktuelle Analysen zeigen zudem, dass eine PTEN-Defizienz bei Patienten mit De-novo-mHSPC, die eine Standardtherapie erhalten, mit einer numerisch kürzeren Zeit bis zum Übergang in ein kastrationsresistentes Stadium assoziiert ist und unabhängig vom Metastasenvolumen ein eigenständiger negativer Prädiktor für das Gesamtüberleben darstellt 16, 17.
Über die reine Prognose hinaus besitzt der PTEN-Status auch Relevanz für die Therapieauswahl. In einer explorativen Analyse der STAMPEDE-Studie im mHSPC konnte gezeigt werden, dass Transkriptom-basierte Signaturen einer PTEN-Inaktivierung mit einer erhöhten Sensitivität gegenüber Docetaxel assoziiert sind 18.
Einen weiteren Schritt in Richtung personalisierte Therapie stellt die gezielte duale Blockade des PI3K / AKT- und AR-Signalwegs dar. In der randomisierten Phase-III-Studie CAPItello-281 führte die Kombination aus dem AKT-Inhibitor Capivasertib und Abirateron bei Patienten mit PTEN-defizientem mHSPC zu einer signifikanten Verlängerung des radiographischen progressionsfreien Überlebens gegenüber Abirateron allein. Post-hoc-Analysen zeigten dabei einen zunehmenden Behandlungseffekt mit steigendem Ausmaß des PTEN-Verlustes 19.
AVPC-Signatur (RB1 / TP53 / PTEN) – molekulare Korrelate einer aggressiven, androgenindifferenten Tumorbiologie
Über den isolierten PTEN-Verlust hinaus existiert eine Subgruppe des Prostatakarzinoms mit besonders aggressiver klinischer Biologie, die unter dem Begriff aggressive variant prostate cancer (AVPC) zusammengefasst wird. AVPC ist primär klinisch definiert und zeichnet sich durch rasche Progression, frühe Metastasierung – häufig viszeral –, PSA-diskordante Verläufe sowie ein frühes Versagen AR-gerichteter Therapien aus.
Molekular lassen sich bei einem relevanten Anteil dieser Tumoren kombinierte Alterationen in zentralen Tumorsuppressorgenen, insbesondere RB1, TP53 und PTEN, nachweisen, die als häufige, aber nicht obligate genetische Korrelate dieses Phänotyps gelten 20, 21.
Biologisch begünstigt der kombinierte Verlust von RB1 und TP53, oftmals in Kombination mit einer PTEN-Inaktivierung, eine ausgeprägte lineäre Plastizität mit Abkehr vom luminal-androgenabhängigen Differenzierungsprogramm. Dies geht mit verminderter AR-Signalabhängigkeit und der Aktivierung alternativer proliferativer Programme einher 22.
Klinisch sind Tumoren mit einem solchen molekularen Profil mit einer ungünstigen Prognose assoziiert, sowohl im kastrationsresistenten als auch zunehmend im hormonsensitiven metastasierten Setting. Gleichzeitig weisen sie eine vergleichsweise höhere Sensitivität gegenüber zytotoxischer Chemotherapie, insbesondere platinhaltigen Regimen, auf 22, 23.
Vor diesem Hintergrund sollte bei Patienten mit klinischem Verdacht auf AVPC eine erneute histologische und molekulare Re-Charakterisierung erfolgen.
Zielgerichtete Therapien gegen tumorassoziierte Zelloberflächenproteine beim metastasierten Prostatakarzinom
Neu identifizierte tumorassoziierte Zelloberflächenproteine des Prostatakarzinoms haben in den vergangenen Jahren wesentlich zur Entwicklung personalisierter, zielgerichteter Therapiestrategien beigetragen. Neben dem prostataspezifischen Membranantigen (PSMA) wurden weitere Zielstrukturen wie Kallikrein-2 (hK2), STEAP1, B7H3 oder DLL3 identifiziert, mit weitestgehend selektiver Expression auf Prostatakarzinom bzw. neuroendokrinen Prostatakarzinomen.
Diese Antigene bilden die Grundlage für unterschiedliche therapeutische Plattformen, insbesondere Radiopharmazeutika, zytotoxische Antikörper-Wirkstoff-Konjugate (ADCs) und T-Zell-Engager.
Radiopharmazeutika
Die PSMA-gerichtete Radioligandentherapie (RLT) mit ^177Lu-Lutetium-vipivotid-tetraxetan ist als personalisierte Therapieoption beim mCRPC nach mit mindestens einem AR-gerichteten Wirkstoff und einer taxanbasierten Chemotherapie etabliert. Auf Basis der PSMAfore-Studie wurde die Substanz jüngst auch für den Einsatz vor Docetaxel zugelassen 24. Die Patientenselektion erfolgt hierbei bildgebungsbasiert mittels PSMA-PET / CT und stellt damit ein paradigmatisches Beispiel für ein theranostisches, biomarkerbasiertes Therapiekonzept dar.
Mehrere retrospektive Analysen und Metaanalysen zeigen, dass höhere SUVs (standard uptake values) im Ausgangs- PSMA-PET, insbesondere SUVmax und SUVmean, mit einem besseren Ansprechen auf ^177Lu-PSMA-Radioligandentherapie und günstigeren Therapieergebnissen wie Progressions-freier und Gesamtüberleben assoziiert sind, was die Bedeutung quantitativer PET-Parameter als prädiktive Biomarker für patientenspezifische Therapieentscheidungen unterstreicht 25.
Limitiert wird die Wirksamkeit der PSMA-gerichteten RLT durch eine primäre oder sekundäre Resistenz, die unter anderem auf einem Verlust oder einer heterogenen Expression des Zielantigens sowie auf tumorintrinsischen Adaptationsmechanismen beruht 26. Hierzu zählen insbesondere die Aktivierung von DNA-Schadens- und Replikationsstressantworten, pathogene Alterationen in TP53 und dem Androgenrezeptor sowie die Aktivierung von PI3K / AKT- und MYC-Signalwegen 24.
Vor diesem Hintergrund zielt die Weiterentwicklung von Radiopharmazeutika darauf ab, eine möglichst hohe, lokal begrenzte zytotoxische Strahlendosis bei gleichzeitiger Schonung gesunden Gewebes zu erzielen. Dies erfordert die Berücksichtigung physikalischer und biochemischer Eigenschaften wie Emissionsart, Reichweite, Halbwertszeit, Zielantigenexpression sowie die Stabilität der Radioliganden im Organismus.
Zudem sind Aspekte der Herstellung und Verfügbarkeit für einen breiten klinischen Einsatz relevant 27. Aktuell werden sowohl PSMA-gerichtete Radioliganden gekoppelt an Alpha-Strahler als auch Radiopharmazeutika gegen alternative Zielstrukturen in klinischen Studien evaluiert.
Der Alpha-Strahler Actinium-225 (^225Ac) zeichnet sich durch eine sehr kurze Reichweite von zwei bis drei Zelldurchmessern aus und ermöglicht eine hochlokalisierte DNA-Schädigung 27. In einer großen retrospektiven multizentrischen Analyse erzielte eine ^225Ac-PSMA-gerichtete RLT ein medianes Gesamtüberleben von 15,5 Monaten sowie ein medianes progressionsfreies Überleben von 7,9 Monaten 28.
Derzeit wird ^225Ac-PSMA-617 prospektiv bei Patienten mit und ohne Vortherapie mit ^177Lu-PSMA-617 oder ^177Lu-PSMA-I&T untersucht (NCT04597411).
Neben PSMA werden weitere Zielantigene adressiert. Ein ^225Ac-markierter Antikörper gegen hK2 (JNJ-69086420) zeigte in einer Phase-I-Studie bei mCRPC ein vielversprechendes klinisches, biochemisches und radiologisches Ansprechen bei akzeptablem Toxizitätsprofil 29.
Zytotoxische Antikörper-Wirkstoff-Konjugate
Zytotoxische Antikörper-Wirkstoff-Konjugate (ADCs) stellen eine weitere Klasse zielgerichteter Therapeutika dar, die aus einem monoklonalen Antikörper, einem Linker und einer hochpotenten zytotoxischen Payload bestehen. Während ADCs bei anderen urologischen Tumorentitäten bereits klinisch etabliert sind, befinden sich entsprechende Konzepte beim Prostatakarzinom überwiegend in frühen klinischen Entwicklungsphasen.
PSMA-gerichtete ADCs zeigten in Phase-I /II-Studien moderate klinische Aktivität mit PSA- und CTC-Ansprechraten bei stark vorbehandelten Patienten. Der ADC ARX517 erzielte in einer Phase-1-Studie einen PSA- und CTC-Rückgang von ≥ 50 % bei etwa der Hälfte der behandelten mCRPC-Patienten 30.
Auch STEAP1-gerichtete ADCs wie DSTP3086S wiesen erste klinische Aktivität mit PSA- und CTC-Ansprechen auf 31. Der klinische Stellenwert dieser Substanzen wird derzeit in weiterführenden Studien definiert.
T-Zell-Engager
T-Zell-Engager ermöglichen eine antigenabhängige Rekrutierung und Aktivierung zytotoxischer T-Zellen. Sie bestehen aus variablen Antikörperfragmenten mit Bindungsstellen für ein tumorspezifisches Antigen und für CD3 auf der T-Zelle 32.
Beim metastasierten Prostatakarzinom zeigte der STEAP1-gerichtete T-Zell-Engager Xaluritamig in einer Phase-I-Studie bei intensiv vorbehandelten mCRPC-Patienten PSA-Rückgänge von ≥ 50 % bei etwa der Hälfte der Patienten sowie eine objektive Ansprechrate von 24 %. Die Substanz wird aktuell in einer Phase-III-Studie im Vergleich zu Cabazitaxel oder einem weiteren AR-gerichteten Wirkstoff evaluiert (NCT06691984).
Darüber hinaus wird der neoadjuvante Einsatz bei Patienten mit Hochrisiko-Prostatakarzinom untersucht, um frühe biologische Effekte unabhängig von einer begleitenden Androgendeprivation zu analysieren (NCT04221542).
Pasritamig ist ein KLK2-gerichteter bispezifischer T-Zell-Engager, der in einer Phase-I-Studie bei stark vorbehandelten Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom eine klinisch relevante antitumorale Aktivität zeigte mit einer bemerkenswert niedrigen Rate von Zytokinfreisetzungssyndromen 33. Auch hier rekrutiert derzeit eine Phase-III-Studie in Deutschland (NCT07164443).
Herausforderungen der zielgerichteten Therapie
Trotz erheblicher Fortschritte in der personalisierten Therapie des metastasierten Prostatakarzinoms bestehen im deutschen Versorgungskontext weiterhin relevante strukturelle Herausforderungen. Ein zentrales Hindernis stellen eingeschränkte und heterogene Testmöglichkeiten dar.
Der Zugang zu umfassender molekularpathologischer Diagnostik (z. B. NGS-basierte Genpanels, Liquid Biopsy, standardisierte PSMA-PET-Quantifizierung) ist regional unterschiedlich ausgeprägt und häufig an universitäre Zentren gebunden. Dies limitiert eine flächendeckende, zeitnahe Identifikation von Biomarkern.
Darüber hinaus ist die Kostenübernahme diagnostischer Tests durch gesetzliche Krankenkassen vielfach unzureichend geregelt. Insbesondere wiederholte molekulare Testungen im Krankheitsverlauf, die zur Erfassung klonaler Evolution und therapieinduzierter Resistenzmechanismen erforderlich wären, sind im klinischen Alltag nur eingeschränkt umsetzbar.
Dies steht im Spannungsfeld zur zunehmenden Evidenz, dass eine repetitive biomarkerbasierte Reevaluation für die rationale Sequenzierung zielgerichteter Therapien notwendig ist.
Eine weitere Limitation ergibt sich aus der ausgeprägten intra- und intertumoralen Heterogenität des Prostatakarzinoms. Einzelne Biopsien oder zeitpunktbezogene Analysen bilden die biologische Vielfalt der Erkrankung häufig nur unvollständig ab.
Hinzu kommen methodische Unterschiede und limitierte Standardisierung diagnostischer Verfahren, die die Vergleichbarkeit und Zuverlässigkeit von Testergebnissen beeinträchtigen können.
Zusammenfassend erfordern diese Herausforderungen eine bessere strukturelle Integration molekularer Diagnostik, klare Erstattungsregelungen sowie die Etablierung standardisierter Testalgorithmen.
Ausblick
Zusammenfassend markieren die hier dargestellten Entwicklungen einen nachhaltigen Paradigmenwechsel in der Systemtherapie des Prostatakarzinoms – weg von uniformen Behandlungspfaden hin zu biologisch fundierten, personalisierten Therapiekonzepten.
Fortschritte in der molekularen Charakterisierung, der funktionellen Bildgebung und der Entwicklung zielgerichteter Wirkprinzipien ermöglichen es zunehmend, therapeutisch relevante Abhängigkeiten des Prostatakarzinoms präzise zu identifizieren und gezielt zu adressieren.
Perspektivisch zeichnet sich ein Übergang von statischen Therapiesequenzen hin zu dynamischen, adaptiven Behandlungsstrategien ab, die die molekulare Evolution des Tumors im Krankheitsverlauf berücksichtigen.
Trotz bestehender struktureller und biologischer Herausforderungen lässt die Dynamik aktueller translationaler und klinischer Programme erwarten, dass individualisierte Therapieentscheidungen künftig früher, präziser und breiter implementiert werden können. Damit eröffnet sich die realistische Perspektive, Wirksamkeit und Verträglichkeit systemischer Therapien weiter zu steigern und das klinische Outcome von Patienten mit metastasiertem Prostatakarzinom nachhaltig zu verbessern.
Prof. Dr. Gunhild v. Amsberg
Literatur unter www.uroforum.de



