Die fortgeschrittene Parkinson-Krankheit (PK) stellt eine besondere klinische Herausforderung dar, da sie sich nicht eindeutig über Krankheitsdauer oder klassische Stadieneinteilungen definieren lässt. Vielmehr ist sie gekennzeichnet durch eine zunehmende Belastung durch motorische Fluktuationen und nicht-motorische Symptome, die unter konventioneller oraler/transdermaler Therapie nicht mehr ausreichend kontrollierbar sind und die Lebensqualität erheblich beeinträchtigen. Vor diesem Hintergrund gewinnen strukturierte Screening-Ansätze und geräteunterstützte Therapien zunehmend an Bedeutung. Der vorliegende Artikel gibt einen praxisnahen Überblick über aktuelle Definitionskonzepte, Screening-Instrumente und etablierte sowie neue Therapieoptionen bei fortgeschrittener PK.
Die fortgeschrittene Parkinson-Krankheit
Derzeit gibt es keine einheitliche einzusetzende Definition der fortgeschrittenen PK [1]. Obwohl mit längerer Krankheitsdauer assoziiert, reicht die Dauer allein für die Diagnose nicht aus. Die häufig angewendete Stadieneinteilung nach Hoehn & Yahr (HY) ist aufgrund der fehlenden Erfassung von motorischen- und nicht-motorischen Fluktuationen und dem Fehlen von Informationen zur Lebensqualität limitiert [2].
Die Movement Disorder Society Unified Parkinson‘s Disease Rating Scale (MDS-UPDRS) mit den Subskalen ist das am weitesten verbreitete klinische Instrument zur Quantifizierung sowohl motorischer als auch nicht-motorischer Symptome in allen Krankheitsstadien [3].
Obwohl in klinischen Studien häufig ein HY-Stadium ab 3 sowie ein MDS-UPDRS-Motor-Score von ≥ 30 als Kennzeichen der fortgeschrittenen PK herangezogen werden, verwenden weder HY noch MDS-UPDRS den Begriff „fortgeschritten“ [4].
Am besten wird die fortgeschrittene PK durch das Vorliegen schwerer, beeinträchtigender motorischer und nicht-motorischer Symptome (NMS) definiert, die durch die orale oder transdermale Standardmedikamente nicht ausreichend kontrolliert werden können und zu einer erheblichen Beeinträchtigung der Alltagsfunktionen sowie der Lebensqualität führen [5, 6].
Zu den motorischen Symptomen gehören behindernde Fluktuationen mit regelmäßigen OFF-Symptomen und Dyskinesien. Kognitive Defizite, psychotische Symptome, Depression, Schmerzen, autonome Dysfunktion oder Stürze sind häufige NMS. Der Verlust von Autonomie und die Notwendigkeit der Unterstützung in der Bewältigung der Aktivitäten des täglichen Lebens komplettieren die fortgeschrittene PK. Nicht-motorische Symptome bleiben häufig unerkannt, obwohl sie die Lebensqualität der Betroffenen stärker beeinträchtigen können als motorische Fluktuationen allein [7].
Screening-Tools für die fortgeschrittene Parkinson-Krankheit
Die Auswahl von Menschen mit Parkinson (MmP) für geräteunterstützende Therapien wird üblicherweise in spezialisierten Parkinson-Zentren mittels standardisierten Auswahlverfahren durchgeführt [8]. Die zeitgerechte Überweisung an spezialisierte Zentren ist jedoch suboptimal, da es nach wie vor schwierig ist, jene MmP zu identifizieren, die für eine geräteunterstützende Therapie in Frage kommen. Geringe Erfahrung oder Schwierigkeiten, den richtigen Zeitpunkt für die Überweisung zu bestimmen, sind Hindernisse. Diese Schwierigkeit ist auf das Fehlen klarer und einfach anzuwendender Kriterien für die Vorauswahl zurückzuführen [9]. Dies führt sowohl zu inadäquaten Überweisungen mit Ablehnung im spezialisierten Zentrum oder zu einer Unterversorgung, womit ein potenziell geeigneter MmP keine Gelegenheit zur Evaluation erhält [8].
Zur Identifikation von MmP, die für geräteunterstützte Therapien in Frage kommen, wurden verschiedene Instrumente und Kriterien entwickelt. Diese Werkzeuge sollen eine frühzeitige und angemessene Steuerung für MmP erwirken, die für Therapieverfahren wie die tiefe Hirnstimulation (THS), die kontinuierliche subkutane Apomorphin-Infusion (CSAI) oder das intestinale Levodopa-Carbidopa-Intestinalgel (LCIG) bzw. Levodopa-Entacapon-Carbidopa-Intestinalgel (LECIG) in Frage kommen.
Die derzeit verfügbaren Screening-Instrumente für geräteunterstützte Therapien sind grundsätzlich wirksam. Dennoch bestehen weiterhin Einschränkungen hinsichtlich Sensitivität, Spezifität und Generalisierbarkeit und kein Instrument sollte die klinische Beurteilung ersetzen.
Ein Beispiel für ein Instrument ist die 5–2–1– Regel (≥ 5 L-DOPA-Einnahmezeitpunkte/Tag oder ≥ 2 h/Tag im OFF oder ≥ 1 Stunde pro Tag störende Dyskinesien) mit Ausschöpfung der oralen/transdermalen Therapie und Einschränkung der Lebensqualität [10].
MANAGE-PD hat im Vergleich zur 5–2–1 Regel eine höhere Sensitivität (98,4 %), jedoch geringere Spezifität (69,5 %), wodurch mehr Kandidaten erfasst werden, aber mit einer höheren Rate an falsch-positiven Ergebnissen [11]. Hier bedarf es noch einer Validierung in geeigneten Parkinson-Populationen [12].
D-DATS (Dutch DAT Screening Tool) übertrifft die 5–2–1 Regel sowohl in der Sensitivität (88 %) als auch in der Spezifität (98 %), allerdings steht die externe Validierung noch aus [13].
Der Einsatz von künstlicher Intelligenz kann zur Unterstützung der Entscheidungsfindung für die geräteunterstützten Therapien der PK und bei der Identifikation geeigneter Kandidaten, dem Monitoring und der personalisierten Therapieplanung behilflich sein.
So zeigte die DELIST-PD-Studie, dass anhand klinischer und demografischer Daten MmP für eine geräteunterstützende Therapie mit hoher Genauigkeit identifiziert werden können. Dabei erreichte das Modell eine Sensitivität von 0,91 und eine Spezifität von 0,88. Zentrale Prädiktoren sind die tägliche OFF-Zeit, L-DOPA Dosis und die Krankheitsdauer. Solche Werkzeuge könnten Neurologinnen und Neurologen mit weniger Erfahrung in der Indikation zur geräteunterstützenden Therapie zukünftig dabei helfen, Überweisungen an spezialisierte Zentren zu optimieren [14].
Geräteunterstützende Therapien
Apomorphin
Apomorphin ist ein potenter, kurz wirksamer Dopaminagonist an den D1- und D2-Rezeptoren. Die CSAI ist als wirksame Therapie zur Behandlung bei Patientinnen und Patienten mit behindernden OFF-Phasen und motorischen Fluktuationen, die gegenüber oraler/transdermaler Medikation refraktär sind, lange anerkannt. Zahlreiche klinische Studien, systematische Übersichtsarbeiten und Langzeitbeobachtungsstudien mit robuster Evidenz haben gezeigt, dass die CSAI in der Lage ist, OFF-Zeit rasch und signifikant, zum Teil bis zu 50 % zu reduzieren und motorische Funktion sowie die Lebensqualität insgesamt deutlich verbessern [15–17]. Langzeitstudien bis zu 10 Jahre zeigen eine anhaltende Wirksamkeit ohne signifikanten Toleranz- oder Wirkverlust [18]. Nächtliche Apomorphin-Infusion verbessert Schlafstörungen bei MmP und Insomnie. Darüber hinaus zeigten sich Trends zu Verbesserungen in anderen Bereichen nicht-motorischer Symptome wie Angst und depressive Symptome [19]. Apomorphin wird im Allgemeinen gut vertragen. Die häufigsten Nebenwirkungen sind Übelkeit, Schläfrigkeit, Blutdruckabfall sowie lokale Hautreaktionen an der Injektionsstelle. Psychiatrische Nebenwirkungen und kognitive Beeinträchtigungen treten seltener auf, können jedoch insbesondere bei Langzeitinfusion vorkommen [20].
Foslevodopa/Foscarbidopa
Foslevodopa/Foscarbidopa ist eine neuartige und hochlösliche Prodrug-Formulierung von L-Dopa/Carbidopa für die kontinuierliche subkutane Infusion. Randomisierte kontrollierte und offene Studien zeigen, dass diese Therapie die ON-Zeit ohne störende Dyskinesien signifikant erhöht, die OFF-Zeit reduziert und im Vergleich zu oralem L-DOPA/Carbidopa die Schlaf- und Lebensqualität verbessert. In einer offenen 52-wöchigen Studie mit 244 Patientinnen und Patienten führte die Behandlung zu einer deutlichen Zunahme der ON-Zeit ohne störende Dyskinesien um 3,8 h und einer Reduktion der OFF-Zeit um 3,5 h[21]. In einer randomisierten kontrollierten Studie berichteten 85 % der MmP über unerwünschte Ereignisse, wobei Reaktionen mit Erythem (27 %), Schmerzen (26 %), Zellulitis (19 %) und Ödeme (12 %) am häufigsten waren [22]. Die meisten dieser Nebenwirkungen waren leicht bis mäßig ausgeprägt und treten häufiger in den ersten 4 Wochen der Optimierungsphase auf [23]. Schwere Nebenwirkungen unter Foslevodopa/Foscarbidopa sind selten und betreffen fast ausschließlich Infektionen oder ausgeprägte Entzündungen an der Infusionsstelle. Systemische schwere Nebenwirkungen sind bislang kaum dokumentiert [24].
LCIG und LECIG
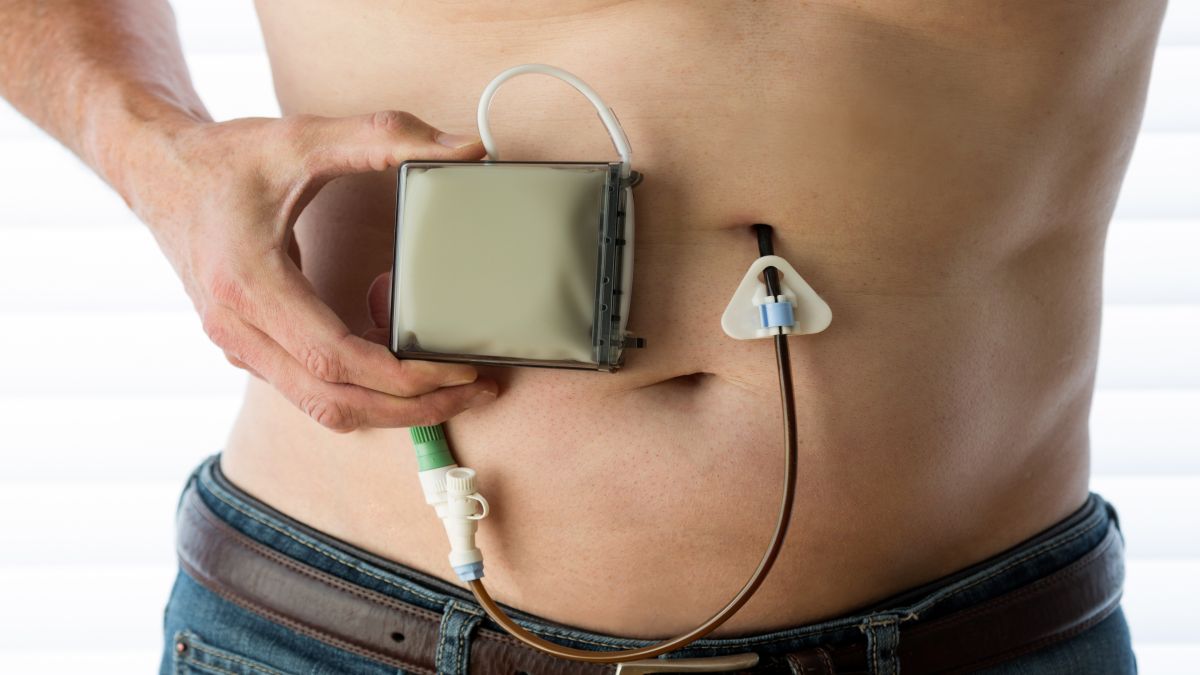
Das Levodopa-Carbidopa-Intestinalgel (LCIG) und das Levodopa-Entacapon-Carbidopa-Intestinalgels (LECIG) werden mit einer Pumpe über eine JET-PEG in das proximale Jejunum appliziert. LCIG verfügt über eine umfangreiche Evidenzbasis, die signifikante und anhaltende Verbesserungen der OFF-Zeit, Dyskinesien, nicht-motorischer Symptome und der Lebensqualität belegt. Das Sicherheitsprofil bei Langzeitanwendung ist gut etabliert [25, 26]. LECIG fügt den COMT-Hemmer Entacapon hinzu. Dadurch erhöht sich die Bioverfügbarkeit von L-Dopa und ermöglicht geringere Tagesdosen sowie ein kleineres Pumpenreservoir. Real-World-Studien zeigen eine vergleichbare Wirksamkeit und Sicherheit zu LCIG.
Sowohl LCIG als auch LECIG führen zu deutlicher und nachhaltiger Reduktion der OFF-Zeit (LCIG: 4–4,4 h/Tag; LECIG: 3,5–3,9 h/Tag), der ON-Zeit ohne störende Dyskinesien (LECIG/LCIG annähernd 4,8 h/Tag), der Lebensqualität und der nicht-motorischen Symptome bei fortgeschrittener PK. Verbesserungen der Lebensqualität stehen in engem Zusammenhang mit der Reduktion motorischer und nicht-motorischer Symptome [27].
Beide intestinalen Gele sind mit Nebenwirkungen verbunden, die meist im Zusammenhang mit dem Infusionssystem (Anlage, Obstruktion, Stoma-Infektion), dem Magen-Darm-Trakt (Gewichtsverlust, Obstipation, Diarrhö und abdominelle Schmerzen) und neuropsychiatrischen Symptomen (Halluzinationen, Psychosen, Stimmungsschwankungen und Agitiertheit) stehen [25, 28].
Dopamin und Vitamin
Bei langfristiger Anwendung von LCIG und LECIG sollte zu Beginn und im Verlauf Vitamin B6/B12, Folat und Homocystein kontrolliert werden. Bei der Methylierung von Dopamin wird S-Adenosylmethionin (SAM) zu Homocystein. Bei der Re-Methylierung von Homocystein zu Methionin ist Folat der Methylgruppendonator und Vitamin B12 Cofaktor. Hohe Abbauraten von Dopamin erfordern damit hohe Mengen an Vitamin B12. Der Abbau von Homocytsein zu Cystein benötigt Vitamin B6 [29]. Polyneuropathien, vermutlich durch B-Vitamin-Mangel bei LCIG sind selten [30, 31]. Für LECIG liegen keine Daten vor [28].
Tiefe-Hirn-Stimulation
Die Ursprünge der Tiefen Hirnstimulation (THS) reichen bis in die 1950er- und 1960er-Jahre zurück, als chronische Elektrostimulation erstmals zur Behandlung psychiatrischer Erkrankungen und von Schmerzen durchgeführt wurde. Die Entwicklung von implantierbaren Herzschrittmachern in den 1970er-Jahren ermöglichte die Konstruktion zuverlässiger, implantierbarer Generatoren und damit die dauerhafte Stimulation subkortikaler Hirnareale.
Ende der 1980er Jahre wurde der entscheidende Wandel in Richtung Bewegungsstörungen durch Stimulation im ventralen intermediären Kern (VIM) des Thalamus bei der Behandlung von Tremor bei Parkinson-Patienten eingeleitet [32].
In den 1990er Jahren wurde die Stimulation des Nucleus subthalamicus (STN) und Globus pallidus internus (GPi) mit deutlichen Verbesserungen der motorischen Symptome eingeführt. Die ersten großen Studien belegten, dass die STN-Stimulation Tremor, Akinese, Rigidität und Dyskinesien wirksam behandeln kann. Die STN-Stimulation kann eine deutliche Reduktion der täglichen L-DOPA Äquivalenzdosis bis 50 % ermöglichen [33].
Indikation für die THS
Die THS ist indiziert für MmP, die unter motorischen Fluktuationen, Dyskinesien oder Tremor leiden, welche durch Medikamente unzureichend kontrolliert werden können, oder die schwerwiegende, durch Medikamente ausgelöste Nebenwirkungen entwickeln [33, 34]. Die THS unterbricht abnormale neuronale Aktivität in den motorischen Regionen der Basalganglien, desynchronisiert überaktive Nervenzellen und moduliert die neuronale Netzwerkdynamik [35]. Bei sorgfältig ausgewählten MmP und ersten motorischen Komplikationen mit gutem Ansprechen auf L-DOPA kann eine frühe THS auch in jungen Lebensjahren die Lebensqualität und die motorischen Symptome signifikant stärker verbessern als die beste medikamentöse Therapie [36]. Ist ein Parkinson-Tremor medikamentös therapierefraktär, kann die THS auch ohne motorische Fluktuationen erwogen werden. Die subjektiv empfundene verminderte Lebensqualität gemessen am Parkinson’s Disease Questionaire (PDQ-39) vor der Implantation ist hierbei der beste Prädiktor für den Therapieerfolg [37]. Die präoperative L-Dopa-Responsivität erlaubt eine Vorhersage für gute Ergebnisse nach der THS [34]. Sprechen die klassischen motorischen Symptome nicht ausreichend auf L-DOPA an, profitieren MmP nicht von einer STN-THS [38]. Die THS ist damit nicht der letzte Strohhalm, sondern ein therapeutisches Zeitfenster, das frühzeitig erkannt und genutzt werden sollte, um keine Jahre in guter Lebensqualität zu verlieren.
THS und Allgemeinanästhesie
Die Implantation des THS-Systems in Allgemeinanästhesie (asleep) ist eine etablierte, sichere und effektive Alternative zur bekannten Wach-OP (awake). Sie bietet insbesondere Vorteile beim Patientenkomfort und ist durch moderne Bildgebungstechniken sehr präzise [39, 40]. Intraoperatives MRT und CT ermöglichen eine sehr präzise Platzierung der Elektroden auch ohne intraoperative Teststimulation am wachen Patienten [41]. So wird die umgangssprachliche Vollnarkose als weniger belastend empfunden und die Operationsdauer ist oft kürzer [39]. Die Allgemeinanästhesie ist besonders geeignet für Patientinnen und Patienten, die eine Wach-OP aus Angst oder Komorbiditäten nicht tolerieren würden.
Kontraindikationen
Patientinnen und Patienten mit deutlichen kognitiven Defiziten haben ein erhöhtes Risiko für ungünstige Ergebnisse und Komplikationen. Schwere, medikamentös nicht behandelbare Depression oder psychiatrische Erkrankung erhöhen das Risiko für neuropsychiatrische Nebenwirkungen und eine schlechte postoperative Anpassung. Schwere Gleichgewichts- und Gangstörungen, häufige Stürze oder Dysarthrie, die nicht auf Medikamente ansprechen, profitieren weniger von der THS [42, 43].
Eine sorgfältige interdisziplinäre Beurteilung durch Neurologie, Neuropsychologie und Neurochirurgie ist für eine optimale Auswahl der MmP unerlässlich.
Interessenkonflikte:
A. Becker erklärt, dass bei der Erstellung des Beitrags keine Interessenkonflikte im Sinne der Empfehlungen des International Committee of Medical Journal Editors bestanden.
Korrespondenzadresse:
Dr. med. Andreas Becker
Chefarzt Neurologie
Ärztlicher Direktor
Kurpfalzkrankenhaus Heidelberg
Tel.: 06221 88–4022
sekretariat_neurologie.kkh@srh.de