Die Parkinson-Krankheit (PK) ist nach der Alzheimer Krankheit die zweithäufigste neurodegenerative Erkrankung und betrifft weltweit über 10 Millionen Menschen [1]. Die PK wird durch das obligatorische Vorhandensein von Bradykinese, sowie Ruhetremor und/oder Rigor definiert, welche eng mit einem Mangel an Dopamin verknüpft sind [2, 3]. Dementsprechend beruhen nahezu alle therapeutischen Ansätze auf einer medikamentösen Modulation des dopaminergen Systems [2]. Allerdings kommt es bei vielen Patientinnen und Patienten im Verlauf zu Komplikationen der medikamentösen Therapie, wie motorischen Fluktuationen, Dyskinesien, Impulskontrollstörungen oder unzureichenden Effekten auf den Tremor [4–6]. Bei diesen Betroffenen kommt häufig die Tiefe Hirnstimulation (THS) zum Einsatz [7].
Mit Ausnahme des Tremors ist es hierbei von besonderer Bedeutung, dass die Symptome, die den Patienten oder die Patientin beeinträchtigen, durch dopaminerge Medikation gebessert werden können, dieser Effekt jedoch über den Tagesverlauf nicht anhält (Fluktuationen) bzw. zu Nebenwirkungen führt (Dyskinesien oder Impulskontrollstörungen). Das Ansprechen auf Levodopa wird routinemäßig präoperativ durch einen Levodopa-Test geprüft, wobei ein deutliches Ansprechen ein wichtiger Prädiktor für den zu erwartenden Effekt der THS ist [8]. Darüber hinaus werden Patientinnen und Patienten auf mögliche Kontraindikation untersucht, wie z. B. dem Vorhandensein einer schweren Depression, Psychose oder Demenz [9].
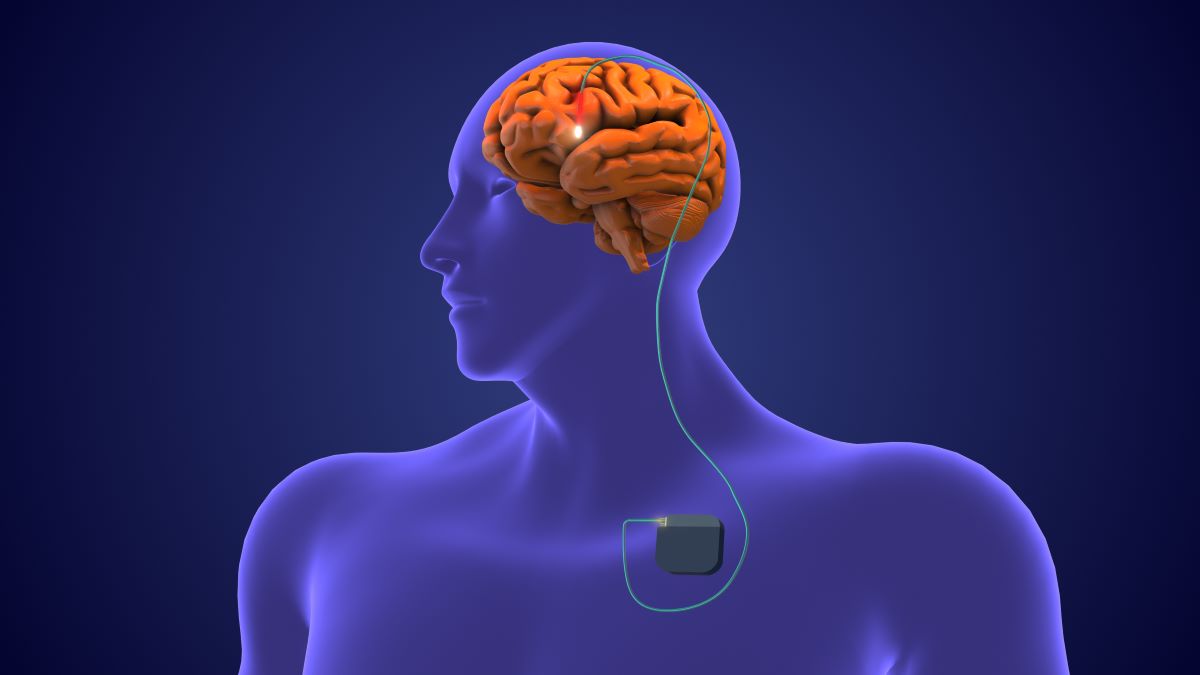
Bei der THS Operation werden Elektroden in tiefliegende Hirngebiete implantiert, im Falle der PK ist das Zielgebiet in der Regel der Nucleus subthalamicus (STN). Die implantierten Elektroden werden dann über ein subkutanes Kabel mit einem Schrittmacher verbunden (▶ Abb. 1, links), über den ein kontinuierlicher Strom gegeben werden kann [10]. Der genaue Mechanismus, mit dem die THS zu einer Linderung der Symptome führt, ist nicht abschließend geklärt. Aktuell geht man von einer Kombination verschiedener Mechanismen wie der lokalen Suppression neuronaler Aktivität, antidromer und orthodromer Modulation verbundener Hirngebiete, sowie der Unterdrückung abnormer rhythmischer Hirnaktivität im Sinne eines Netzwerkeffektes aus [11].

Abb. 1: Überblick Tiefe Hirnstimulation. Links: Die implantierten Elektroden werden über ein subkutanes Kabel mit dem pektoralen Schrittmacher (implantable pulse generator) verbunden. Mitte: Die Kontakte sind typischerweise auf 4 vertikalen Ebenen angeordnet. Bei der Parkinson-Krankheit bzw. dem Nucleus subthalamicus als Zielgebiet haben die 1,5 mm langen Kontakte einen Abstand von 0,5 mm. Bei der Einstellung wird getestet welcher Kontakt bzw. welche Kontakte für optimale klinische Effekte aktiviert werden müssen (im Bild ist der 2. unterste Kontakt aktiviert; aktivierter Kontakt und induziertes Stromfeld sind in rot illustriert). Rechts: Segmentierte Elektroden (im Bild der 2. unterste und 2. oberste Kontakt) erlauben es, das Stromfeld direktional zu steuern. In diesem Bild ist einer der segmentierten Kontakte nicht aktiviert (z. B. wenn Nebenwirkungen bei Aktivierung des Kontaktes auftreten), sodass das Stromfeld in die entgegengesetzte Richtung gesteuert wird (in Rot illustriert).
Die THS ist ein etabliertes und leitliniengerechtes Verfahren zur Behandlung der PK sowie anderen Bewegungsstörungen wie Essenziellem Tremor oder Dystonie und wird zunehmend auch bei neuropsychiatrischen Erkrankungen wie der Zwangserkrankung eingesetzt [7]. Tendenziell wird die THS zunehmend in früheren Krankheitsphasen der PK eingesetzt, da der klinische Effekt bei gut ausgewählten Patientinnen und Patienten der besten medizinischen Behandlung überlegen ist [12, 13]. Allerdings ist es wichtig, dass die klinische Diagnose gesichert ist, da z. B. bei atypischen Parkinson Syndromen die THS nicht effektiv ist.
Postoperativ kann die dopaminerge Medikation in der Regel erheblich – durchschnittlich um ca. 50 % – reduziert werden, wobei deutliche inter-individuelle Unterschiede bestehen [7, 10]. Die postoperative Optimierung der THS wird typischerweise in regelmäßigen ambulanten Kontrollterminen durchgeführt, wobei insbesondere überprüft wird, welcher Kontakt der THS Elektrode aktiviert werden soll, (auf der THS-Elektrode befinden sich mehrere vertikal angeordnete Kontakte, im STN typischerweise auf 4 vertikalen Ebenen von 1,5 mm Länge, die 0,5 mm voneinander entfernt sind, (▶ Abb. 1 Mitte), welche Intensität gewählt werden soll (meist 2–5 mA) und mit welcher Frequenz und Impulsbreite der Strom appliziert wird (typischerweise 130 Hz bei 40–90 µs). Die häufigsten Nebenwirkungen der THS sind eine Stimulations-induzierte Dysarthrie, Parästhesien und Muskelkontraktionen [7, 14]. Die THS steht bereits seit über 30 Jahren zur Behandlung der PK zur Verfügung [15]. Über die letzten Jahre gab es wichtige neue Entwicklungen dieses Therapieverfahrens, auf welche wir im Folgenden eingehen werden.
Wiederaufladbare Systeme
Die subkutan meist im Bereich unterhalb des Schlüsselbeins implantierten Schrittmacher waren zunächst stets nicht-wiederaufladbare Systeme ähnlich einer Batterie mit einer vorgegebenen Kapazität. Die Dauer, bis die Kapazität aufgebraucht ist, hängt maßgeblich von den Stimulationseinstellungen ab, die benötigt werden, um eine effektive Therapie zu gewährleisten. Bei PK ist mit einer Batterielebensdauer von meist 3–5 Jahren zu rechnen [16]. Der Batteriestand kann von Patientinnen und Patienten über das Handgerät bedarfsgerecht abgefragt werden und informiert bei bald drohender Batterieerschöpfung. Ein operativer Schrittmacherwechsel stellt einen kleinen Eingriff dar, der meist in Lokalanästhesie mit milder Sedierung durchgeführt wird. Damit stellen Schrittmacherwechsel den häufigsten Folgeeingriff für Menschen mit THS-Therapie dar. Da die THS eine lebenslange Therapie ist und Patientinnen und Patienten tendenziell im jüngeren Lebensalter implantiert werden, stellen wiederholte Schrittmacherwechsel eine Herausforderung dar. Die Rate an Wundinfektionen steigt ab dem 3. Wechsel stark auf mehr als 20 % an [17], was eine Explantation des Systems zur Folge haben kann.
Daher wurden wiederaufladbare THS-Schrittmacher ähnlich einem Akku entwickelt, welche seit den 2010er Jahren verfügbar sind. Meist ist das Implantatvolumen der wiederaufladbaren Systeme kleiner, da die Akkukapazität geringer ausfallen kann als die der entsprechenden nicht-wiederaufladbaren Batterie. Die verfügbaren wiederaufladbaren Schrittmacher können 15–25 Jahre eingesetzt werden, bevor Sie ausgetauscht werden müssen, wodurch sich die Anzahl an Folgeoperationen deutlich reduziert. Patientinnen und Patienten müssen ebenfalls mit dem Handgerät die Akkukapazität überprüfen und können dann mit einem Ladegerät, welches mithilfe eines Gurtes im Bereich des Schrittmachers platziert wird, den Schrittmacher induktiv aufladen. In einer multizentrischen Studie konnte gezeigt werden, dass Patientinnen und Patienten mit PK durchschnittlich eine Ladelast von 90 Minuten pro Woche aufweisen. Die Handhabung wurde von den anwendenden Personen als leicht eingestuft und es gab nur in 4 % der Fälle temporäre Unterbrechungen der Stimulation durch fehlgeschlagene oder versäumte Ladungen [18].
Telemetrie
Ambulante Wiedervorstellungstermine zur Anpassung der Stimulationseinstellungen stellen bei der PK die häufigsten Kontakte zwischen Klinik und Patientinnen und Patienten dar. Hierbei werden meist kleinere Anpassungen der Stimulation vorgenommen, welche keinen hohen Zeitaufwand bedeuten. An- und Abreisewege von und zur Klinik, sowie Wartezeiten können für die Betroffenen jedoch einen erhöhten Aufwand darstellen.
Es steht ein THS-System zur Verfügung, bei welchem eine Fernprogrammierung und Televisite stattfinden kann (Abbott Neurosphere Virtual ClinicTM). Hierbei können Patientin bzw. Patient und die Behandler einen virtuellen Ambulanztermin vereinbaren, zu dem sich beide Parteien mit Ihren Hand- bzw. Programmiergeräten über eine sichere Internetverbindung einwählen. Während diesem virtuellen Ambulanztermin besteht zum einen eine Videoverbindung, was die Kommunikation und die visuelle Beurteilung von motorischen Symptomen ermöglicht, zum anderen ist es den Behandelnden möglich, auf die Einstellungen des Schrittmachers zuzugreifen und die Stimulationsparameter anzupassen. Kommt es während einer solchen Visite zu einer Unterbrechung der sicheren Internetverbindung, so wird automatisch die letzte Stimulationseinstellung vor der Visite wieder aktiviert.
In einer randomisierten Studie konnte gezeigt werden, dass nach Implantation des THS-Systems PK-Patientinnen und Patienten mittels der Televisiten ca. 14 Tage schneller eine zufriedenstellende Einstellung erzielen konnten verglichen mit den üblichen Klinikvisiten [19], wobei im Durchschnitt jedoch mehr Kontakte mittels der Televisite verglichen mit den Klinikvisiten notwendig waren.
Televisiten können für PK-Betroffene eine Erleichterung hinsichtlich Zeit- und Kostenaufwand darstellen. Dieser Effekt betrifft Länder mit größerer Fläche und geringerer Klinikdichte wie z.B. Kanada umso mehr [20].
Bild-gesteuerte Anpassungen der THS
Technologische Weiterentwicklungen der implantierten Elektroden erlauben seit einigen Jahren die Stimulation nicht nur omnidirektional, d. h. in alle Richtungen ausgehend über eine Stimulation der Ringelektroden, sondern auch gerichtet, d. h. nach anterior, medial oder lateral, zu geben. Hierzu wurden segmentierte Elektroden, die an den beiden mittleren Kontakten der THS eine direktionale Stimulation ermöglichen, entwickelt, ▶ Abbildung 1 rechts. In der klinischen Praxis hat sich dies bereits als hilfreich erwiesen, da sich so ein größeres therapeutisches Fenster ergibt, in dem klinische Symptome gelindert werden können, ohne dass es zu Nebenwirkungen kommt [21].
Die Ersteinstellungen der THS werden typischerweise weiterhin omnidirektional über Ringstimulation getestet, um zu ermitteln, auf welcher vertikalen Ebene die besten klinischen Effekte bzw. die geringsten Nebenwirkungen erzielt werden können, um so die Anzahl an möglichen Stimulationskontakten und damit die Dauer der THS-Testung zu begrenzen. Ergeben sich hierbei suboptimale Effekte, welche sich oft erst im Verlauf der ambulanten Kontrollen zeigen, kann eine Testung der Stimulation über die direktionalen Kontakte erfolgen. Kommt es z. B. zu einer Reizung der Capsula interna und damit verbundenen Muskelkontraktionen, kann getestet werden ob bei Reduktion der lateralen Stimulation (also Inaktivierung des segmentierten Kontaktes, der nach lateral ausgerichtet ist) diese Nebenwirkung gemindert werden kann. Studien haben gezeigt, dass ca. 50 % der Patienten im Langzeitverlauf solch eine direktionale Stimulation erhalten [22]. Bei manchen THS-Geräten ist es möglich, den Anteil des Stromes, welcher über jeden Kontakt gegeben werden kann, zu bestimmen, sodass Kontakte nicht nur aus- oder angeschaltet werden können, sondern das induzierte Stromfeld noch genauer gelenkt werden kann.
Eine neue Software (Boston Scientific Illumina 3D®) ermöglicht es den Ärztinnen und Ärzten vorzugeben, welche Hirnregion optimal stimuliert werden sollte (bei der PK wäre dies typischerweise im dorsolateralen STN) und die Software errechnet selbst, welche Einstellungen vorgenommen werden sollte, um diesen Effekt zu erreichen. Hierfür werden die Bildinformationen des präoperativen MRTs, sowie die postoperativen CT-Daten benötigt, welche mittels automatischer Segmentierung von Hirnregionen und der Bildfusion der Elektrodenlage und -rotation innerhalb der Zielstruktur ein realitätsnahes Modell darstellen können. Erste Studien weisen darauf hin, dass solch eine bild-gesteuerte Anpassung der THS die Einstellungen weiter erleichtern kann [23].
Adaptive THS
Ziel der adaptiven THS ist es, dass Stimulationsparameter automatisch angepasst werden ohne dass hierzu eine klinische Kontrolle notwendig ist [24]. Grundprinzip ist hierbei, dass ein Signal, welches im Sinne eines Biomarkers den klinischen Zustand der Betroffenen widerspiegelt, mit einem optimalen Wert dieses Biomarkers verglichen wird und bei Abweichungen die Stimulation so angepasst wird, dass diese Abweichung minimiert wird [11, 24]. Sowohl die Stimulation als auch Messungen der neuronalen Aktivität können über die implantierten Elektroden durchgeführt werden, siehe ▶ Abbildung 2. Das am besten getestete Feedback Signal bei der PK ist die Amplitude von STN Aktivität im Beta Bereich (13–30 Hz), da diese mit der Ausprägung von Bradykinese und Rigor korreliert [24, 25]. Überschreitet dieses Signal einen festgelegten Grenzwert, wird die Stromstärke der THS erhöht, während bei Unterschreiten eines Grenzwertes die Stromstärke vermindert wird. Erste Studien zur adaptiven THS zeigten vielversprechende Ergebnisse. So konnten die motorischen Symptome der PK durch die adaptive THS mindestens genauso gut reduziert werden wie bei der klinisch-angewandten kontinuierlichen THS, obwohl nur zu ca. die Hälfte der Zeit stimuliert wurde [26], wodurch auch verminderte Nebenwirkungen in Form der Dysarthrie erreicht werden konnten [14].
2025 wurde das erste THS System, welches adaptive THS implementiert, zugelassen (Medtronic Percept®) und die adaptive THS hat Eingang in die klinische Praxis gefunden. Aktuelle Ansätze zur Weiterentwicklung der adaptiven THS zielen vor allem darauf ab, das Feedback Signal für die Anpassungen zu erweitern, sodass nicht nur STN Beta Aktivität, sondern auch andere Marker inkludiert werden können [27], sowie ein Anpassen der THS auf zirkadiane Rhythmen zu ermöglichen [28].

Abb. 2: Adaptive Tiefe Hirnstimulation. Über die implantierten Elektroden kann neuronale Aktivität als Feedback Signal gemessen werden (in Blau). Bei Abweichungen dieses Feedback Signals von vorgegebenen Werten kann die Stimulation angepasst werden (in Rot). Aktivität wird bipolar von Kontakten, die um den aktiven Kontakt liegen, abgeleitet um das Stimulationsartefakt zu minimieren (rechts im Bild).
Literatur:
- Luo Y et al. „Global, regional, national epidemiology and trends of Parkinson‘s disease from 1990 to 2021: findings from the Global Burden of Disease Study 2021,“ Front Aging Neurosci 2024; 16: 1498756
- Bloem BR et al. „Parkinson‘s disease,“ Lancet 2021; 397: 2284–303
- Jenkinson N & Brown P. „New insights into the relationship between dopamine, beta oscillations and motor function,“ Trends Neurosci 2011; 34:. 611–8
- F. Baig et al. „Impulse control disorders in Parkinson disease and RBD: A longitudinal study of severity,“ Neurology, vol. 93, no. 7:. e675-e687, Aug 13 2019.
- Hauser RA. „Levodopa: past, present, and future,“ Eur Neurol 2009; 62: 1–8
- Nutt JG & Holford NH. „The response to levodopa in Parkinson‘s disease: imposing pharmacological law and order,“ Ann Neurol 1996; 39, no. 5: 561–73
- Krauss JK et al. „Technology of deep brain stimulation: current status and future directions,“ Nat Rev Neurol 2021;. 17(2): 75–87
- Lachenmayer ML et al. „Subthalamic and pallidal deep brain stimulation for Parkinson‘s disease-meta-analysis of outcomes,“ NPJ Parkinsons Dis 2021; 7(1): 77
- Reese R et al. „Invasive therapies for Parkinson‘s disease: an adapted excerpt from the guidelines of the German Society of Neurology,“ J Neurol 2025; 272(3): 219
- Okun MS. „Deep-brain stimulation for Parkinson‘s disease,“ N Engl J Med 2012: 367(16): 1529–38
- Neumann WJ et al. „Neurophysiological mechanisms of deep brain stimulation across spatiotemporal resolutions 2023;; 11: 4456–68
- Schuepbach WM et al. „Neurostimulation for Parkinson‘s disease with early motor complications,“ N Engl J Med 2013;. 368(7): 610–22
- A. Williams et al. „Deep brain stimulation plus best medical therapy versus best medical therapy alone for advanced Parkinson‘s disease (PD SURG trial): a randomised, open-label trial,“ Lancet Neurol 2010; 9(6): 581–91
- Little S et al. „Adaptive deep brain stimulation for Parkinson‘s disease demonstrates reduced speech side effects compared to conventional stimulation in the acute setting,“ J Neurol Neurosurg Psychiatry 2016; 201; 87(12): 1388–9
- Benabid AL et al. „Long-term suppression of tremor by chronic stimulation of the ventral intermediate thalamic nucleus,“ Lancet 1991; 337(8738): 403–6
- van Riesen C et al. „Disease-specific longevity of impulse generators in deep brain stimulation and review of the literature,“ J Neural Transm (Vienna) 2016; 123(6): 621–30
- Thrane JF et al. „Increasing infection rate in multiple implanted pulse generator changes in movement disorder patients treated with deep brain stimulation,“ Stereotact Funct Neurosurg 2014; 92(6): 360–4 2014,
- M. Jakobs et al. „A multicenter, open-label, controlled trial on acceptance, convenience, and complications of rechargeable internal pulse generators for deep brain stimulation: the Multi Recharge Trial,“ J Neurosurg 2020; 133(3): 821–9
- A. Gharabaghi et al. „Accelerated symptom improvement in Parkinson‘s disease via remote internet-based optimization of deep brain stimulation therapy: a randomized controlled multicenter trial,“ Commun Med (Lond) 2025; 5(1)
- Fung WKW et al. „Remote Deep Brain Stimulation Programming in Canada,“ Mov Disord Clin Pract 2024; 11(5): 586–9
- Dembek TA et al. „Directional DBS increases side-effect thresholds-A prospective, double-blind trial,“ Mov Disord 2017; 32(10): 1380–8
- A. Schnitzler et al. „Directional Deep Brain Stimulation for Parkinson‘s Disease: Results of an International Crossover Study With Randomized, Double-Blind Primary Endpoint,“ Neuromodulation 2022; 25(6): 817–28
- Torres V et al.„Image-guided programming deep brain stimulation improves clinical outcomes in patients with Parkinson‘s disease,“ NPJ Parkinsons Dis 2024; 10(1): 29
- Meidahl AC et al., „Adaptive Deep Brain Stimulation for Movement Disorders: The Long Road to Clinical Therapy,“ Mov Disord 2017; 32(6): 810–9
- Little S & Brown P. „What brain signals are suitable for feedback control of deep brain stimulation in Parkinson‘s disease?,“ Ann N Y Acad Sci 2012; 1265(1): 9–24
- S. Little et al. „Adaptive deep brain stimulation in advanced Parkinson disease,“ Ann Neurol 2013; 74(3): 449–57
- Oehrn CR et al. „Chronic adaptive deep brain stimulation versus conventional stimulation in Parkinson‘s disease: a blinded randomized feasibility trial,“ Nat Med 2024; 30(11): 3345–56
- 28.. M. Herz DM et al. „Low-Frequency Deep Brain Stimulation in Non-Rapid Eye Movement Sleep Modifies Memory Retention in Parkinson‘s Disease,“ Mov Disord 2025; 40(2): 285–91
Interessenskonflikte:
Dr. D. M. Herz erklärt, dass bei der Erstellung des Beitrags keine Interessenkonflikte im Sinne der Empfehlungen des International Committee of Medical Journal Editors bestanden. Prof. M. Jakobs erklärt, Beratertätigkeiten für Medtronic und Vortragtätigkeit für Boston Scientific ausgeführt hatte.
© mgo fachverlage, all rights reserved
Korrespondenzadresse:
Dr. Dr. med. Damian M. Herz
Klinik für Neurologie
Sektion Neurodegeneration
Universitätsklinikum Heidelberg
Im Neuenheimer Feld 400
69120 Heidelberg
Prof. Dr. med. Martin Jakobs
Klinik für Neurochirurgie
Sektion stereotaktische Neurochirurgie
Universitätsklinikum Heidelberg
Im Neuenheimer Feld 400
69120 Heidelberg