Eine klinische Studie zeigt, dass CAR-T-Zellen mit Stammgedächtnis-Phänotyp bereits bei niedrigen Dosen komplette Remissionen erzielen – auch ohne chemotherapeutische Vorbehandlung.
Die CAR-T-Zelltherapie hat die Behandlung bestimmter Blutkrebserkrankungen revolutioniert. Allerdings profitieren viele Patienten bisher nicht dauerhaft, weil die übertragenen CAR-T-Zellen sich meist nicht ausreichend vermehren oder dauerhaft im Körper verbleiben. Um diese Hindernisse zu überwinden, haben die Wissenschaftler in ihrer neuen Studie T-Stammgedächtniszellen (TSCM -Zellen) verwendet. Gattinoni und sein Team hatten dafür eine Plattform-Technologie zur Herstellung solcher CAR modifizierter TSCM-Zellen für den klinischen Einsatz etabliert und deren überlegene Wirksamkeit an Modellen der akuten lymphoblastischen Leukämie (ALL) gezeigt.
„Aktuelle CAR T Produkte können stark variieren, und diese Heterogenität zeigt sich dann in unterschiedlichen Therapieerfolgen und Toxizitäten. Deshalb haben wir ein standardisiertes CD8+ CAR-T-Zellprodukt mit genau definierten Eigenschaften entwickelt, das gezielt mit TSCM-Zellen angereichert ist, und es mit konventionellen CAR-T-Zellen verglichen“, sagt Gabriele Inchingolo, Doktorand in Gattinonis Team und gemeinsamer Erstautor.
Was die Plattform zur Herstellung CAR modifizierter TSCM-Zellen zeigte
Wie die Studie zur Behandlung in Patienten mit rezidivierten oder refraktären CD19+ B-Zell Erkrankungen nach allogener hämatopoetischer Stammzelltransplantation zeigte, vermehrten sich die CAR modifizierten TSCM-Zellen stärker und überlebten länger als Standard CAR-T-Zellen. So kam es zu kompletten Remissionen bei niedrigen Dosen – und das sogar ohne die sonst übliche lymphodepletierende Chemotherapie vor der Infusion. „Die Zellen, die aus der TSCM Plattformtechnologie stammten, führten im Blut der Patienten zu einem höheren CAR-T-Zellspiegel – und in vielen Studien waren hohe CAR-T-Zellspiegel im Blut ein starker Prädikator für klinischen Erfolg“, lautet die Einschätzung von Dr. James Kochenderfer, Ko-Autor und leitender Wissenschaftler in der Abteilung für Chirurgie des National Cancer Institute (NCI) in Bethesda, USA. „Dass Patienten bei Dosen von nur 250.000 Zellen/kg komplette Tumorrückbildungen erreichen, ganz ohne chemotherapeutische Vorbehandlung, bestätigt jahrelange Vorarbeit und eröffnet neue Möglichkeiten im CAR T Zelldesign“, ergänzt Gattinoni.
Das TSCM-Zellprodukt war zudem gut verträglich. „In dieser Studie kam es zu weniger Zytokinfreisetzungs-Syndromen als in den meisten anderen CAR Studien, an denen ich beteiligt war“, berichtet Kochenderfer. Das Zytokinfreisetzungs Syndrom (CRS) ist eine häufige und potenziell schwerwiegende entzündliche Reaktion des Immunsystems, die ausgelöst wird, wenn CAR-T-Zellen im Körper aktiv werden. Selbst bei CAR-T-Zellmengen, die in der Vergleichsgruppe zu schweren CRS führten, traten bei TSCM Behandelten meist nur milde Nebenwirkungen auf. Das deutet darauf hin, dass das TSCM Produkt CAR-T-Zellen bildet, welche die sonst damit verbundenen schweren Nebenwirkungen nicht auslösen.
Zugleich zeigte die Studie, wie unterschiedlich sich die Zellprodukte im menschlichen Körper verhalten: Anders als konventionelle CAR-T-Zellen, die ihre stammzellähnlichen Reserven aufbrauchen, erhalten CAR-TSCM-Zellen während der gesamten Therapie ein beständiges, Reservoir, das sich über einen allmählichen Austausch aktiver Klone erneuert. „Die TSCM Zellen werden also nicht alle gleichzeitig aktiviert, sondern in kleinen aufeinanderfolgenden Wellen. Nacheinander werden unterschiedliche Klone aktiv, sodass das Gesamtreservoir ruhender, stammzellähnlicher Zellen erhalten bleibt. Zum ersten Mal sehen wir dieses Grundprinzip direkt im Menschen“, erklärt Dr. Enrico Lugli, Ko-Autor der Studie und Projektleiter im Labor für translationale Immunologie und Leiter der Core Facility Durchflusszytometrie am Humanitas Research Hospital in Rozzano, Italien.
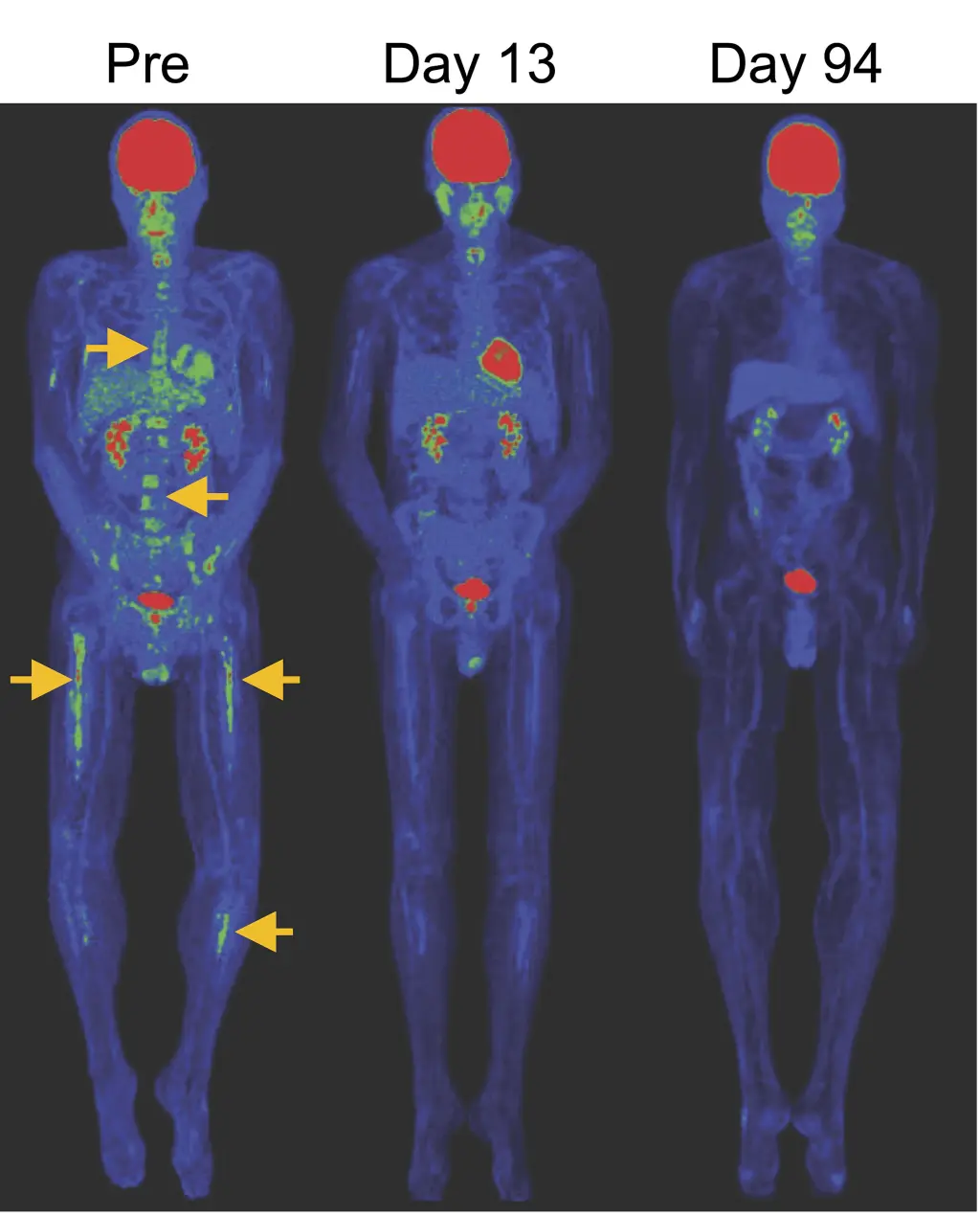
Studiendesign
Die Phase 1 Studie (NCT01087294) unter Leitung von Dr. James Kochenderfer am US-amerikanischen NIH rekrutierte Patienten mit rezidivierten oder refraktären CD19+ B-Zell Erkrankungen nach allogener hämatopoetischer Stammzelltransplantation, also eine Patientengruppe mit wenigen Therapieoptionen. Zwei aufeinanderfolgende Kohorten erhielten entweder konventionelle allogene CD19 CAR-T-Zellen oder angereicherte CAR-TSCM-Zellen. Alle Infusionen erfolgten ohne lymphodepletierende Chemotherapie und ermöglichten es den Wissenschaftlern so, die beiden Zellprodukte direkt zu bewerten.
Das Immunmonitoring wurde vom LIT koordiniert und in Zusammenarbeit mit Humanitas Wissenschaftlern durchgeführt, die Patienten longitudinal mit multidimensionaler Durchflusszytometrie und Bioinformatik nachverfolgten, um Expansion, Persistenz und Schicksal der CAR-T-Zellen zu kartieren. Wie bei Frühphasenstudien üblich, müssen diese Ergebnisse in größeren, randomisierten Studien bestätigt werden, um die klinische Aussagekraft des TSCM-Ansatzes zu belegen.
Ausblick
Wichtige Erkenntnisse gewannen die Forscher auch bei den Patienten, bei denen das TSCM-Produkt in der Studie nicht anschlug: Denn die Ursachen für das jeweilige Therapieversagen waren weniger die T-Zellen selbst, sondern externe Faktoren wie etwa ein geringes Vorkommen des Zielproteins auf den Tumorzellen, immunsuppressive Signale (insbesondere Interleukin 10) oder Immunantworten gegen die CAR Konstrukte.
„Wir haben gezeigt, dass ein klar definiertes, stammzellähnliches Zellprodukt bei niedrigeren Dosen wirksam sein kann. Mit einer homogenen TSCM Population können wir vermutlich eine verlässlichere Ansiedlung und Persistenz von CAR-modifizierten T-Zellen erreichen und so besser vorhersehbare Ergebnisse sowie zielgerichtetere klinische Studien planen“, fasst Gattinoni zusammen.
Das volle Potenzial von CAR TSCM-Zellen ist mit dieser Studie noch nicht vollständig erschlossen: Zukünftige Studien mit lymphodepletierender Chemotherapie, vollständig humanisierten CAR Konstrukten und möglicher Ergänzung durch CD4+ T-Zellen dürften die Therapieerfolge weiter verbessern. Die hier gewonnenen biologischen Erkenntnisse sind wahrscheinlich auch außerhalb des post-alloHSCT-Settings relevant – etwa für autologe CAR-T-Zelltherapien und bei soliden Tumoren, bei denen die Erschöpfung der CAR-T-Zellen bislang die Wirksamkeit begrenzte.
Originalpublikation: Gattinoni L, Inchingolo G, Harrer D et al. Distinct in vivo dynamics of donor-derived stem cell memory CAR-T-cells post-allogeneic HSCT relapse. Cell. 2026
Quelle: Pressemitteilung Leibniz-Institut für Immuntherapie
Bildunterschrit: Prof. Dr. Luca Gattinoni und Gabriele Inchingolo (links)



