Seit 2022 besteht durch die Zulassung von Pembrolizumab auch beim Nierenzellkarzinom die Möglichkeit einer adjuvanten Therapie für Patienten mit einem erhöhten Metastasierungsrisiko [1]. Wird aber auch jeder Risikopatient behandelt und was sind die Gründe, weshalb darauf verzichtet wird?
Die Standardtherapie für Patienten mit lokal begrenzten Nierenzellkarzinomen ist die operative Tumorentfernung entweder mittels Nierenteilresektion oder bei größerer Ausdehnung die Nephrektomie 2, 3.
Mit steigendem Tumorstadium und dem Auftreten von Lymphknoten- oder Fernmetastasen verschlechtert sich die Prognose der Patienten deutlich 4.
Während der Großteil der Patienten mit lokalbegrenzten Nierenzellkarzinomen durch die Operation allein geheilt wird, entwickeln bis zu 20 % der Patienten im weiteren Verlauf Metastasen 5.
Verbessertes Überleben durch adjuvante Therapie
Für Patienten mit Nierenzellkarzinom und hohem Risiko für einen Progress ist seit 2022 eine adjuvante Therapie mit Pembrolizumab zugelassen 1. Im Rahmen der Zulassungsstudie Keynote-564 wurden die Patienten in drei Risikogruppen eingeteilt (intermediate-high risk, high risk und M1 NED), die der Therapie zugeführt wurden 6.
Als intermediate-high risk galten Tumore des Stadiums pT3 oder pT2-Tumore mit sarkomatoider Differenzierung oder schlechtem Grading (G4) 6. High-risk-Tumore waren definiert als pT4 und / oder lymphonodal metastasiert unabhängig vom T-Stadium. Die M1-NED-Gruppe setzte sich aus metastasierten Patienten zusammen, die durch die Tumor- und Metastasenresektion „tumorfrei“ wurden 6.
Durch diese Therapie konnte in der Studie ein signifikant längeres krankheitsfreies Überleben (DFS) und Gesamtüberleben (OS) erreicht werden 7, 8.
Anzumerken ist hierbei, dass in der Studie etwa 86 % der Patienten in die intermediate-high- Gruppe, aber nur 7 % in die high risk-Gruppe fielen 6. Während nach 24 Monaten über 70 % der Patienten der intermediate-high risk-Gruppe auch ohne Therapie rezidivfrei blieben, betrug dieser Anteil in der high risk-Gruppe nur etwa 35 % 9.
Die absolute Risikoreduktion betrug bei 24 Monaten etwa 10 % für die intermediate-high risk Gruppe 9. Da der Großteil der Patienten in die intermediate-high risk Gruppe fiel, stellt sich die Frage, ob wirklich jeder Risikopatient adjuvant behandelt werden sollte, da dies zu einer erheblichen Übertherapie führt.
Dies ist von hoher Relevanz, da Pembrolizumab zu erheblichen Nebenwirkungen (Grad 3 oder höher) bei etwa einem Drittel der Patienten führte und 21 % der Patienten deshalb die Therapie abbrechen mussten 9.
Reale Daten zur Behandlungsrate
Aus diesem Grund haben wir untersucht, wie hoch die tatsächliche Behandlungsrate ist, und sind der Frage nachgegangen, weshalb keine Therapie erfolgte.
Im Zeitraum von Januar 2022 bis Juli 2025 wurden in unserer Klinik 404 Patienten mit Nierentumor operiert, von denen 319 (79 %) ein Nierenzellkarzinom aufwiesen. Lediglich 51 Patienten (16 %) fielen in die intermediate-high- und high-risk-Risikogruppen gemäß der Keynote-564-Studie.
Auch in unserer Analyse stellten die intermediate-high risk-Patienten mit einem Anteil von 90,2 % den Großteil des Kollektivs dar. Bei 22 Patienten (43,1 %) wurde die Therapie durchgeführt, bei 29 Patienten erfolgte diese jedoch nicht.
Nach Patientenauskunft wurde die Therapie bei 8 Patienten (27,6 %) nicht durch den Hausurologen empfohlen. Bei einem Patienten erfolgte keine Nachsorge (3,4 %). Weitere Gründe waren ein schlechter Allgemeinzustand (6,9 %), relevante Komorbiditäten (17,2 %), ein zu langer Zeitraum bis zum möglichen Therapiebeginn (6,9%), hohes Alter (6,9%) sowie der Verdacht auf Metastasen (6,9 %).
Ein Patient hat die Behandlung abgelehnt. Bei 6 Patienten konnte kein Grund eruiert werden (▶ Abb.).
Ähnlich wie bei Rojas et al. 10 und bei Campi et al. 11 weist in unserer Studie nur ein geringer Teil der Patienten mit lokal begrenztem Nierenzellkarzinom ein Metastasierungsrisiko entsprechend der Definition der Keynote-564-Zulassungsstudie auf, wobei nur wenige Patienten in die höchste Risikogruppe fallen.
Trotz Leitlinien-basierter Empfehlung durch unsere Klinik erhielten nur 43 % tatsächlich eine adjuvante Therapie. Einfluss auf die Entscheidung hatte neben Komorbiditäten auch die individuelle Patientenberatung.
Hierbei sollte jedoch berücksichtigt werden, dass die Gründe aus Patienten- und nicht aus Behandlersicht erhoben wurden. Die Auskünfte der Behandler könnten hier durchaus weitere Erkenntnisse liefern.
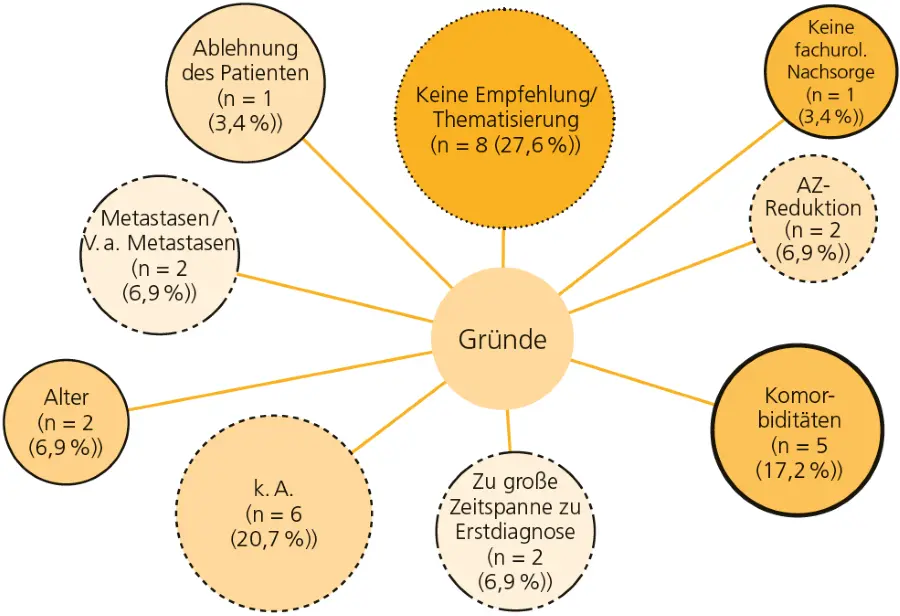
Faktoren der Therapieentscheidung
Interessant ist in diesem Zusammenhang eine Arbeit von Vass et al. 12, die untersuchte, welche Faktoren die Behandlungsentscheidung von Urologen und Onkologen bei der adjuvanten Therapie anhand hypothetischer Fälle beeinflussten.
Eindrücklich war hierbei, dass in diesen hypothetischen Szenarien zwar rund 75 % zugunsten eines höheren OS und DFS eine adjuvante Therapie präferierten, jedoch auch knapp 25 % der Behandler davon Abstand nahmen. Hierbei konkurrierte bei letzteren die therapieassoziierten Nebenwirkungen mit dem zu erwartenden OS-Vorteil 12.
Ähnliche Tendenzen konnten auch bei Patienten erhoben werden, wobei hier der Anteil der Ablehnung der adjuvanten Therapie mit 35% größer war 13. Patienten favorisierten Behandlungen, die das DFS und OS verlängerten, seltener genommen werden müssen, keine weitere Medikation benötigen, kürzer dauern und ein geringeres Nebenwirkungspotential haben 13.
Knapp 65 % der befragten Patienten waren zu Kompromissen und der Inkaufnahme von Nebenwirkungen bereit, wenn hierdurch das OS oder PFS verbessert werden konnte 13.
In Zusammenschau mit unseren Daten scheint gerade in der intermediate-high-risk-Patientengruppe eine individuelle Beratung über den nachweislichen Nutzen, aber eben auch über das Risiko der Übertherapie und Nebenwirkungen besonders wichtig, da ein Großteil dieser Patienten auch ohne Therapie rezidivfrei bleiben würde, wie in der Keynote-564 Studie belegt.
Wer profitiert von Behandlung?
Deshalb ist eine bessere Patientenstratifizierung dringend erforderlich, um schließlich die Patienten zu selektieren, die tatsächlich ein hohes Risiko aufweisen und von der Therapie profitieren. Dies würde auch die individuelle Beratung durch die behandelnden Ärzte erleichtern.
Neben der hauptsächlich histopathologisch fokussierten Risikoeinteilung wie in der Keynote-564 Studie oder anderen Scores wie dem SSIGN-Score 14 oder dem Leibovich-Score 15 sollten weitere Faktoren einbezogen werden, die die Metastasierung beeinflussen.
In den letzten zehn Jahren wurden mehrere molekulare Signaturen entwickelt und zum großen Teil unabhängig validiert, die das Metastasierungspotential der Primärtumoren definieren. So hat unsere Arbeitsgruppe einen genetischen Prognosescore entwickelt, der neben der T-Kategorie die chromosomalen Veränderungen miteinbezog und dem Leibovich-Score überlegen war 16.
Darüber hinaus wurden Genexpressionssignaturen wie der 16-Gene Score 17 und der ClearCode34 erstellt 18 . Auch miRNA-Signaturen erwiesen sich als prognostisch bedeutsam, wie auch von uns und anderen Gruppen gezeigt wurde 19, 20. Obwohl die prognostische Wertigkeit und Überlegenheit im Vergleich zu klinischen Parametern und Scores vielfach belegt wurde, haben diese molekularen Signaturen noch keinen Einzug in die Leitlinien und damit die Behandlungsrealität gefunden.
Diese müssten daher zukünftig in klinische Studien zur adjuvanten Therapie integriert werden, um eine individualisierte Therapie zu ermöglichen und damit die Über-, aber auch Untertherapie für Patienten, die nicht in die klinisch definierten Risikogruppen fallen, zu reduzieren.
Ob auch Marker aus dem Blut, wie KIM-1 oder ctDNA wie für Harnblasen- und Kolonkarzinome diskutiert, zur Risikostratifierung bzw. frühzeitigen Erkennung der Metastasierung geeignet sind, muss weiter untersucht werden. Darüber hinaus werden aber auch prädiktive Marker benötigt, die das Ansprechen auf die Therapie individuell vorhersagen können.
Dr. Clara Sophia Jungfleisch
Literatur unter www.uroforum..de



