Das Nierenzellkarzinom (NZK) zählt zu den häufigsten malignen Tumoren des Urogenitaltrakts und weist eine ausgeprägte biologische wie molekulare Heterogenität auf [1]. Während die Forschung der vergangenen Jahre vor allem genetische Mechanismen der Tumorprogression und immunonkologische Aspekte beleuchtet hat, blieb die Rolle des Tumorstromas – insbesondere fibrotischer Umbauvorgänge – weitgehend unbeachtet [2]. Dabei ist bekannt, dass Fibrose in vielen Organen nicht nur reparative Reaktionen, sondern auch Tumorentstehung und -progression beeinflussen kann [3].
Im Bereich der Nierenmalignome existieren bisher lediglich Einzelfallbeobachtungen oder indirekte Hinweise auf Zusammenhänge zwischen Stromaarchitektur, Fibrose und Tumorbiologie 4. Für die klinische Praxis der Urologie ergeben sich jedoch wichtige Fragen:
Hat ein stark fibrotisches Tumorstroma Einfluss auf die Aggressivität und das biologische Verhalten des Tumors?
Wirkt sich Fibrose auf das Ansprechen systemischer Therapien aus – insbesondere auf VEGF-basierte antiangiogene Ansätze und Immuncheckpoint-Inhibitoren?
Kann die Analyse der Fibrose helfen, Tumorsubtypen besser zu differenzieren oder Prognosen präziser abzuschätzen?
Ziel unserer Arbeit war daher die integrative morphologische, molekularpathologische und transkriptomische Analyse der intratumoralen Fibrose in unterschiedlichen Subtypen des NZK. Besonderes Augenmerk lag auf der Interaktion zwischen Tumorzellen, stromalen Fibrosemarkern und endothelialen Signaturen.
Kohorte und histologische Analysen
Insgesamt wurden 70 Nierenzellkarzinome unterschiedlicher Subtypen – klarzellig, papillär und chromophob – mittels klassischer Pathologie, digitaler Immunfluoreszenz, RNA-Sequenzierung und Proteomanalyse untersucht. Zur immunhistochemischen und immunfluoreszenten Charakterisierung wurden folgende Marker quantifiziert:
Alpha-SMA (α-smooth muscle actin) – Marker der myofibroblastischen Aktivierung
CD31 (PECAM-1) – Endothelzellmarker
Kollagen Typ I – struktureller Marker extrazellulärer Matrixbildung
Im Rahmen der Immunfluoreszenz wurde die Marker-Expression digital erfasst und als prozentuale Markerfläche analysiert.
Für eine Subkohorte wurde frisch gewonnenes Tumorgewebe einer umfassenden molekularen Charakterisierung unterzogen. Die RNA-Sequenzierung umfasste:
Transkriptomanalysen von Tumorgewebe
Identifikation differenziell exprimierter Gene
Analysen von Transkriptionsfaktor-Aktivitäten (TF)
Zuordnung von TF-Clustern zu fibrotischen Markern (Collagen I, Alpha-SMA, CD31)
Zudem wurden die Transkriptionsfaktorprofile von zehn klarzelligen NZK mit der immunfluoreszenten Quantifizierung von Alpha-SMA, CD31 und Kollagen I korreliert.
Ergebnisse
Immunfluoreszenz
Zwischen den Subtypen ergaben sich deutliche Unterschiede in der endothelialen Signatur:
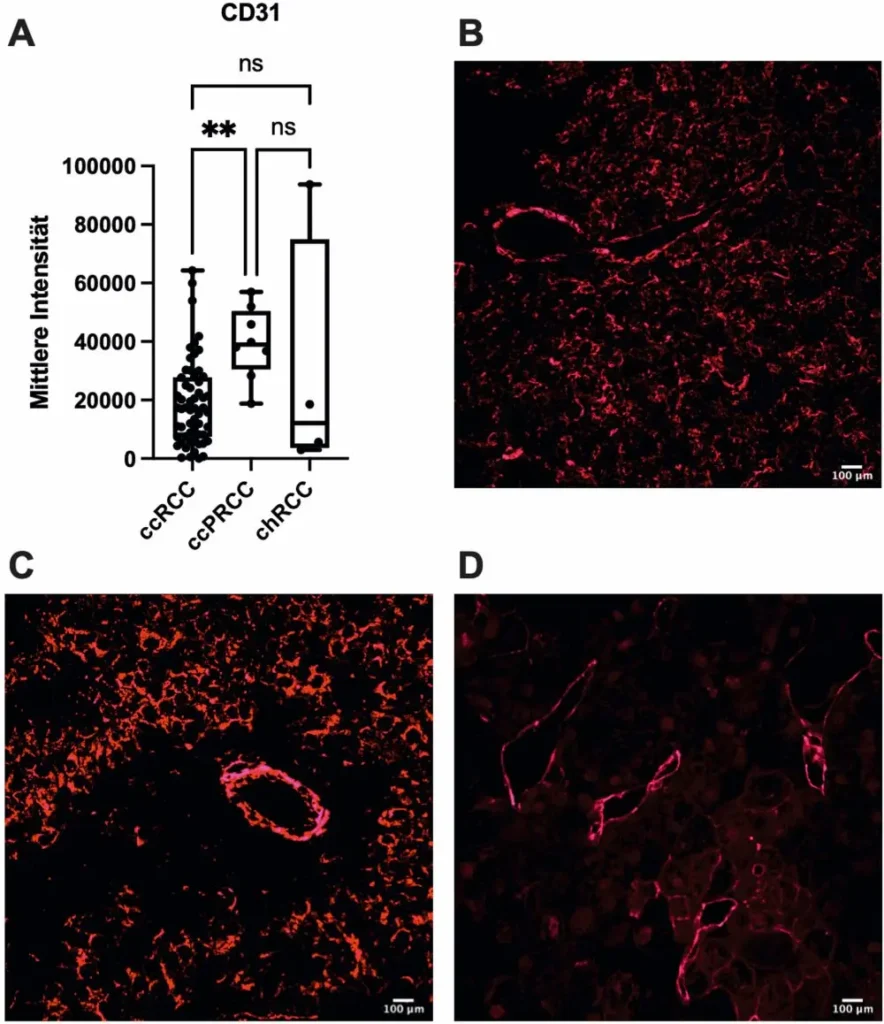
CD31 war bei papillären NZK signifikant höher exprimiert als bei klarzelligen Tumoren (▶ Abb. 1). Dies weist auf Unterschiede in der vaskulären Architektur sowie der stromalen Organisation hin. Die Expression von Alpha-SMA und Kollagen I war innerhalb aller Subtypen heterogen, jedoch zeigten insbesondere klarzellige NZK klar abgegrenzte Areale mit ausgeprägtem fibrotischem Umbau.
Transkriptomische Analysen
Die RNA-Sequenzierung zeigten deutliche Unterschiede in Matrix-remodellierenden Genclustern, eine veränderte Aktivität zentraler Transkriptionsfaktoren sowie konsistente regulatorische Verbindungen zwischen TF-Clustern und den Fibrosemarkern Alpha-SMA, CD31 und Kollagen I.
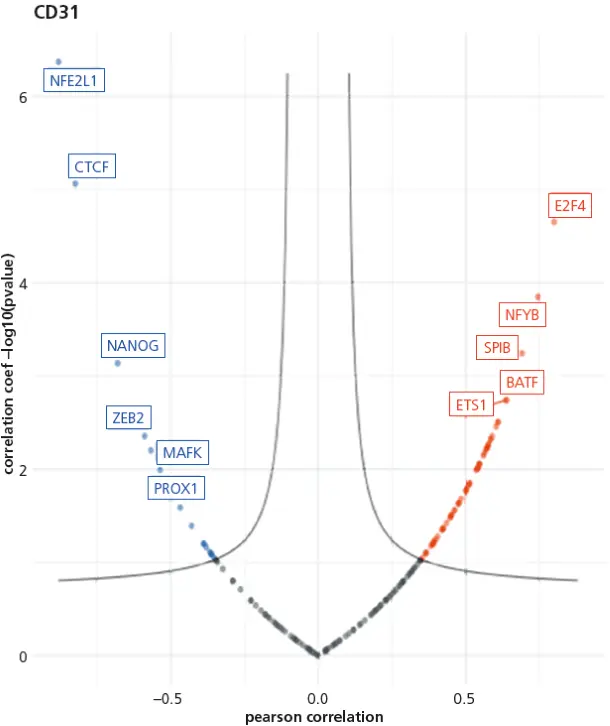
Exemplarisch ist in Abbildung 3 (S. 20) die Assoziation verschiedener Transkriptionsfaktoren mit CD31 dargestellt. Diese Ergebnisse sprechen für eine funktionelle Interaktion zwischen Tumorzellen und fibrotischem Stroma – nicht lediglich für ein begleitendes Umbauphänomen.
Cluster-Interaktionen
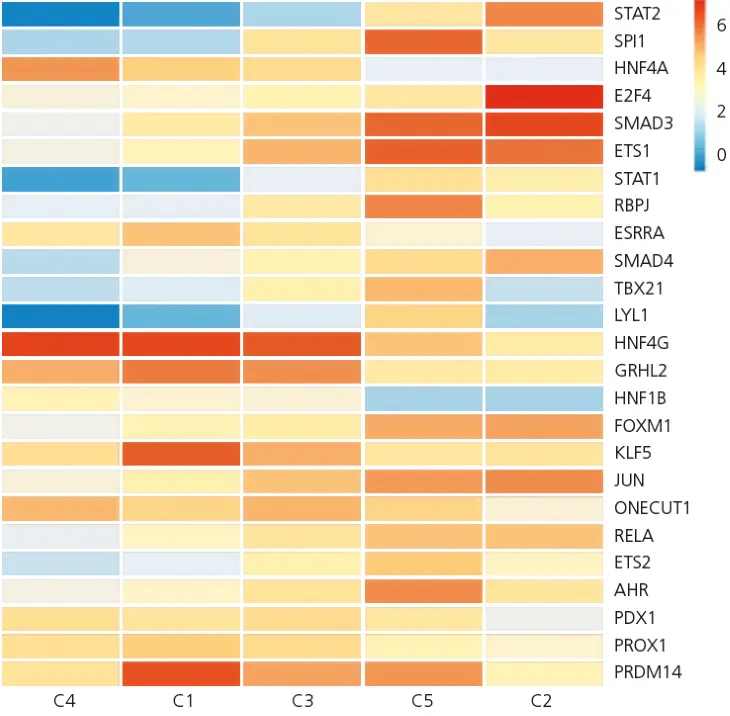
Basierend auf der Kollagen-I-Expression wurden fünf molekulare Cluster identifiziert (▶ Abb. 2). Cluster 2 und 5 wiesen eine erhöhte Fibroseaktivität auf, Cluster 1, 3 und 4 eine deutlich geringere Aktivität. Diese Cluster unterschieden sich auf transkriptomischer Ebene und veranschaulichen, dass Fibrose ein regulierter biologischer Prozess im Tumor ist – nicht lediglich ein unspezifisches Endstadium.
Diskussion
Klinische Relevanz für die Urologie
Die intratumorale Fibrose wird in der Diagnostik des NZK bisher kaum berücksichtigt und findet weder in aktuellen Klassifikationssystemen noch in Risikomodellen Beachtung. Unsere Ergebnisse zeigen jedoch, dass fibrotische und endotheliale Marker – insbesondere CD31 – relevante strukturelle und molekulare Hinweise auf Tumorverhalten und Subtypcharakteristika liefern können.
Das erhöhte CD31-Vorkommen bei papillären NZK ist besonders interessant, da es auf eine stärker endothelialisierte Tumormikroumgebung hinweist 5. Dies könnte für ein potenziell besseres Ansprechen papillärer Tumore auf antiangiogene Therapien sprechen, welche primär eine vaskuläre Normalisierung erzeugt.
Die Kombination endothelialer und fibroblastischer Aktivität eröffnet neue Perspektiven für die Prognoseeinschätzung, subtypspezifische Therapieplanung sowie das Verständnis immunologischer Interaktionen innerhalb der Tumormikroumgebung.
Auch die proteomischen Daten liefern Hinweise, dass die Fibrose im NZK einen aktiven Bestandteil der Tumorökologie darstellt und möglicherweise als zukünftiges therapeutisches Co-Targets genutzt werden könnte – insbesondere im Rahmen der Präzisionsmedizin.
Schlussfolgerung
Die Bedeutung fibrotischer Signalwege im Nierenzellkarzinom wird bislang unterschätzt. Unsere Studie zeigt, dass intratumorale Fibrose wertvolle strukturelle und molekulare Informationen über Tumorbiologie und Subtypverhalten liefert.
Für zukünftige Entwicklungen erscheint es sinnvoll, Fibroseparameter in größeren Kohorten zu untersuchen und für risikoadaptierte Klassifikationen zu integrieren. Die Identifikation fibrotischer Tumoreigenschaften könnte langfristig einen Beitrag zur personalisierten Diagnostik und Therapie des NZK leisten und klinisch tätigen Urologinnen und Urologen zusätzliche Entscheidungshilfen bieten.
Literatur unter www.uroforum.de
Dr. Felix Steffens



